Жидкое состояние – это одно из основных состояний вещества, предшествующее газообразному и следующее за твердым состоянием. Жидкость объединяет в себе свойства и характеристики твердого и газообразного состояний, обладая как некоторой подвижностью, так и отсутствием определенной формы.
Одной из особенностей жидкостей является их способность сохранять объем, но занимать форму сосуда. Частицы в жидкости находятся в очень близком контакте, но не имеют строго определенного порядка расположения.
В жидкости взаимодействие между частицами является существенным, поэтому они могут образовывать когерентные области. Это объясняет явление поверхностного натяжения - способность жидкости образовывать пленку на своей поверхности.
Хотя жидкости имеют большую плотность по сравнению с газами, их частицы все равно обладают большим движением, что обусловлено некоторой свободой, характерной для данного состояния.
Жидкости широко используются во многих сферах нашей жизни, начиная от химических реакций и технологических процессов, заканчивая бытовым использованием в виде питательных и гигиенических веществ.
Жидкое состояние: понятие и свойства
Первым характерным свойством жидкости является ее способность принимать форму сосуда, в котором она находится. Это связано с тем, что молекулы жидкости находятся близко друг к другу и обладают достаточной подвижностью для того, чтобы занимать любую форму сосуда. В то же время, они сохраняют относительно постоянное распределение и не меняют своих положений в пространстве.
Второе важное свойство жидкостей - их плотность. Плотность жидкостей обычно выше, чем плотность газов, но меньше, чем плотность твердых веществ. Это связано с близким расположением молекул жидкости друг к другу, что обеспечивает их высокую плотность.
Еще одно характерное свойство жидкостей - их способность к течению. Благодаря свободному перемещению молекул друг относительно друга, жидкость может легко протекать и занимать форму сосуда, в котором она находится. Это делает жидкости очень удобными для транспортировки и использования в различных областях нашей жизни.
Также стоит отметить, что жидкости обладают поверхностным натяжением – свойством проявлять силы притяжения на поверхности и образовывать пузырьки и капли. Это объясняется взаимодействием между молекулами на поверхности жидкостей и приводит к образованию таких явлений, как капиллярность и всплеск.
Таким образом, жидкое состояние вещества характеризуется свободным перемещением молекул, способностью принимать форму сосуда и обладает такими свойствами, как плотность, способность к течению и поверхностное натяжение. Эти свойства делают жидкости важными и широко используемыми веществами в нашей повседневной жизни.
Жидкость: определение и химическая природа

Жидкость обладает такими характерными свойствами, как течение и поверхностное натяжение. Однако, в отличие от газов, она не расширяется до бесконечности и не настолько сжимаема, как твердые вещества.
Химическая природа жидкости зависит от вида вещества. Вода является наиболее распространенной жидкостью на Земле. Она состоит из молекул, состоящих из атомов кислорода и водорода, объединенных ковалентными связями. Вода обладает рядом уникальных свойств, таких как высокое покрытие поверхности насосов и силы адгезии, что делает ее одним из ключевых растворителей и идеальным средством для поддержания жизни.
Кроме воды, существует множество разных типов жидкостей с различной химической природой. Некоторые из них являются органическими соединениями, такими как алкоголи, кетоны и эфиры, другие - неорганическими веществами, такими как серная кислота и ртути.
Каждая жидкость имеет свои уникальные свойства и применения в различных отраслях промышленности и науки. Изучение химической природы жидкостей важно для понимания их свойств и использования их в различных процессах и экспериментах.
Физические свойства жидкости

Основные физические свойства жидкости включают:
| Вязкость | Жидкость обладает вязкостью, то есть способностью сопротивляться деформации под действием внешней силы. Она может быть вязкой (с высокой вязкостью) или текучей (с низкой вязкостью). |
| Плотность | Плотность жидкости определяет ее массу, содержащуюся в единице объема. Она обычно измеряется в г/см³ или кг/м³. Плотность может изменяться в зависимости от давления и температуры. |
| Коэффициент поверхностного натяжения | Это свойство жидкости, которое определяет ее поверхностное состояние и способность образовывать пленку на поверхности. Коэффициент поверхностного натяжения зависит от химического состава и температуры жидкости. |
| Теплопроводность | Жидкость обладает теплопроводностью - способностью передавать тепло. Ее значения могут различаться в зависимости от вещества. |
| Теплоемкость | Теплоемкость жидкости определяет количество теплоты, необходимое для изменения ее температуры. Она может быть различной в зависимости от вещества. |
Эти свойства важны при изучении и использовании жидкостей в различных областях науки и технологии, таких как химия, физика, медицина, пищевая промышленность и другие.
Фазовые переходы: из твердого в жидкое состояние
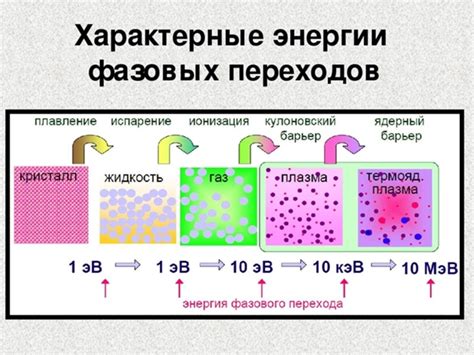
Плавление осуществляется при повышении температуры, когда кристаллическая решетка вещества начинает колебаться и перемещаться. Это позволяет межчастичным силам преодолеть силы удерживающие их в твердом состоянии. Таким образом, вещество переходит в более хаотичное и движущееся состояние, что характерно для жидкости.
Факторы, влияющие на температуру плавления вещества, включают силу притяжения между атомами или молекулами, а также их размеры и форму. Сильные межмолекулярные силы требуют более высоких температур для разрушения и преодоления, поэтому вещества с высокими температурами плавления являются более устойчивыми в твердом состоянии.
Плавление также зависит от давления. При повышении давления пространство между молекулами уменьшается, что подавляет их движение и усиливает притяжение. Поэтому для плавления вещества может потребоваться более высокая температура при высоком давлении.
Важно отметить, что плавление - это обратимый процесс, и вещество может снова стать твердым при снижении температуры. Этот процесс называется затвердеванием или кристаллизацией. Во время кристаллизации частицы приобретают упорядоченное положение и сформируют кристаллическую решетку.
Понимание фазовых переходов из твердого в жидкое состояние позволяет подробно изучить свойства веществ и определить оптимальные условия для различных процессов и применений.
Жидкое состояние идеального газа
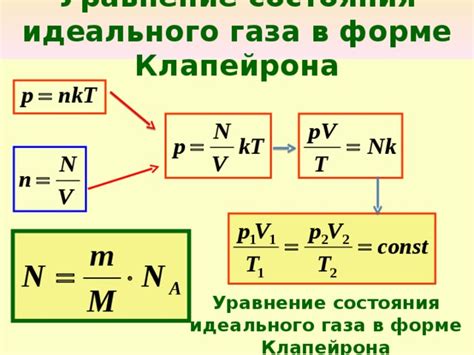
Идеальный газ, в отличие от реальных газов, не образует жидкость при достижении критической температуры. Вместо этого, идеальный газ переходит непосредственно из газообразного состояния в твердое состояние путем замерзания.
Однако, при снижении температуры идеальный газ может приближаться к своей критической температуре, наблюдаясь пренебрежимо малое количество газа в жидком состоянии. Приближаясь к критической температуре, межмолекулярные силы становятся все более существенными, давая возможность образования небольших скоплений молекул, напоминающих жидкость.
Вместо отдельных молекул, в жидком состоянии идеального газа образуется сферическое скопление, называемое "димер", состоящее из двух молекул газа, которые временно оказываются связанными друг с другом. В жидком состоянии идеального газа такие димеры могут перемещаться, сталкиваться или распадаться под воздействием теплового движения.
| Свойство | Жидкое состояние идеального газа |
|---|---|
| Форма | Принимает форму сосуда, в котором находится |
| Объем | Определенный объем, не пропускающий другой газ |
| Плотность | Высокая плотность по сравнению с газообразным состоянием |
| Движение молекул | Молекулы движутся свободно и непрерывно, сохраняясь внутренняя энергия между ними |
| Силы притяжения | Межмолекулярные силы притяжения сравнительно слабы |
Жидкое состояние идеального газа имеет промежуточные характеристики между газом и жидкостью, поэтому его часто называют "сверхкритическим газом". Это состояние газа может быть установлено при очень высоких давлениях и/или очень низких температурах.
Жидкое состояние идеального газа является важным объектом исследования в химии и физике, поскольку его свойства и поведение помогают понять более сложные системы, такие как реальные жидкости и газы. Понимание жидкого состояния идеального газа позволяет разрабатывать новые материалы и технологии, а также решать различные задачи в науке и промышленности.
Жидкость: поверхностное натяжение и вязкость

Поверхностное натяжение - это явление, характерное для жидкостей, заключающееся в том, что свободная поверхность жидкости ведет себя как ограниченная упругой пленкой. Поверхностное натяжение возникает из-за преобладания сил притяжения молекул внутри жидкости по сравнению с силами притяжения молекул жидкости к соседним молекулам воздуха или другой среды. Это явление позволяет жидкости принимать определенную форму и образовывать капли.
Вязкость - это свойство жидкости сопротивляться деформации под воздействием сдвиговых напряжений. Вязкость обусловлена внутренним трением между слоями жидкости при ее течении. Различные жидкости могут иметь различную вязкость, что определяется их внутренней структурой и молекулярными силами. Вязкость влияет на скорость распространения потока жидкости и определяет ее текучесть.
| Свойство | Поверхностное натяжение | Вязкость |
|---|---|---|
| Описание | Поведение свободной поверхности жидкости | Сопротивление деформации и текучесть жидкости |
| Причина возникновения | Силы притяжения внутри жидкости и к соседним средам | Внутреннее трение между слоями жидкости |
| Влияние на свойства | Определяет форму свободной поверхности и образование капель | Влияет на скорость потока и текучесть жидкости |
Жидкость: капиллярное действие и когезия
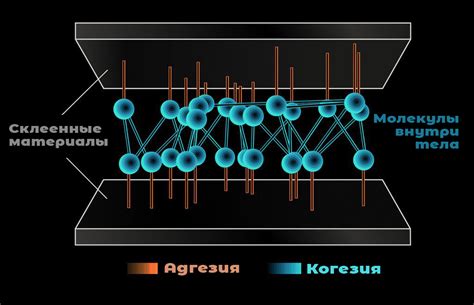
Капиллярное действие - это способность жидкости проникать в тонкие капилляры или пористые материалы. Это свойство обусловлено силой поверхностного натяжения, которая возникает на границе раздела жидкости с другой средой, например, с воздухом или твердым телом. Капиллярное действие играет важную роль во многих процессах, таких как впитывание в жидкость чернил при письме пером, подъем влаги в растениях или движение крови в сосудах живых организмов.
Когезия - это силы, связывающие между собой молекулы одной и той же жидкости. Когезия влияет на форму и поверхностное натяжение жидкости. Вода обладает высокой когезией благодаря водородным связям между молекулами воды. Это свойство позволяет воде образовывать капли и позволяет жидкости сохранять свою форму в определенных условиях.
Когезия и капиллярное действие являются важными свойствами жидкости, которые определены структурой и взаимодействием молекул вещества. Изучение этих свойств помогает понять различные явления, которые происходят с жидкостями в естественных и технических процессах.



