Химия - это наука о веществах и их свойствах, о реакциях, происходящих между веществами. Один из ключевых понятий в химии - это понятие основания. Основания играют важную роль в химических реакциях и имеют свои характерные свойства.
Основания - это вещества, которые способны в щелочной реакции принимать протоны и образовывать соли. Они обладают рядом характеристических признаков, по которым их можно определить. Одним из таких признаков является способность основания выделять отрицательные ионы гидроксида (OH-) в растворе.
Если вещество образует гидроксидионы в растворе и обладает щелочными свойствами, то, скорее всего, это основание. Другими словами, основание - это вещество, способное при растворении в воде образовывать гидроксидные ионы.
Основание в химии: что это такое и как его определить?
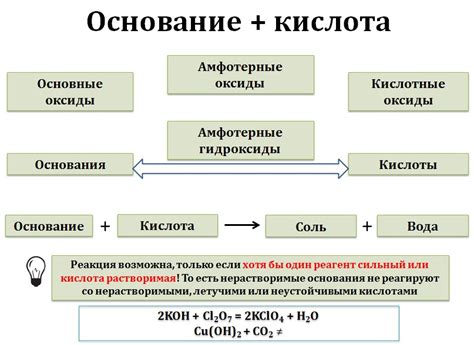
Одним из способов определения основания является изучение его pH-значения. Основание характеризуется высоким pH (больше 7), что означает, что оно обладает щелочными свойствами. Щелочные растворы и вещества могут нейтрализовать кислоты и образовывать соли. Например, гидроксид натрия (NaOH) является сильным основанием, имеющим pH около 14. Оно образует щелочные растворы и используется в многих промышленных и лабораторных процессах.
Еще одним способом определения основания является его реакция с кислотой. Основание реагирует с кислотой, образуя соль и воду в химической реакции, которая называется нейтрализацией. При этой реакции основание отдает свои электроны или принимает протоны от кислоты, образуя новые химические связи и продукты.
Основания широко используются в нашей повседневной жизни. Они присутствуют в бытовых товарах, таких как моющие средства и щелочные батарейки. Они также используются в промышленности, медицине и агрокультуре.
Основание в химии: определение и классификация
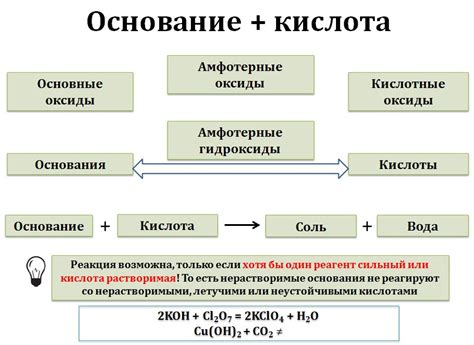
Основание в химии определяется как вещество, способное взаимодействовать с кислотой и образовывать соль и воду. Оно обладает рядом химических свойств, которые определяют его классификацию.
Основания можно классифицировать по различным критериям, включая реактивность, растворимость, электронную структуру и pH-значение. Наиболее распространенная классификация оснований основывается на их реактивности и свойствах.
| Класс | Описание |
|---|---|
| Амфотерные основания | Основания, которые могут реагировать как с кислотами, так и с основаниями |
| Растворимые основания | Основания, которые полностью растворяются в воде |
| Нерастворимые основания | Основания, которые не растворяются в воде |
| Сильные основания | Основания, которые полностью диссоциируют в водном растворе |
| Слабые основания | Основания, которые частично диссоциируют в водном растворе |
Кроме того, основания могут быть классифицированы по своей электронной структуре, включая анионные, катионные и нейтральные основания. Анионные основания содержат отрицательно заряженные ионы, катионные - положительно заряженные ионы, а нейтральные основания не содержат заряда.
Основания играют важную роль во многих химических реакциях и процессах. Изучение и классификация оснований помогает понять их свойства и влияние на окружающую среду.
Химические реакции, связанные с основаниями

Классическим примером химической реакции, связанной с основаниями, является нейтрализация. В ходе нейтрализации основание и кислота соединяются, образуя соль и воду. Обычно эта реакция сопровождается выделением тепла.
К примеру, реакция нейтрализации между гидроксидом натрия (NaOH) и соляной кислотой (HCl) может быть представлена уравнением:
NaOH + HCl → NaCl + H2O
Такие реакции широко используются в промышленности, медицине и повседневной жизни. Например, нейтрализация чрезвычайно полезна в лекарственной промышленности для производства лекарств, и в домашних условиях для приготовления различных продуктов.
Основания также могут участвовать в других химических реакциях, например, образовании осадков. Когда основание реагирует с солью, могут образоваться осадки в виде новых соединений.
Важно помнить, что основания могут обладать различными свойствами и реагировать с разными веществами по-разному. Поэтому изучение свойств оснований и их химических реакций имеет важное значение для химиков и исследователей в данной области.
Методы определения оснований

Существуют различные методы определения оснований, включая:
| Метод | Описание |
|---|---|
| Кислотно-основное титрование | Определение концентрации основания путем титрования с известным объемом кислоты. |
| Использование индикаторов | Изменение цвета индикатора позволяет определить точку эквивалентности реакции между кислотой и основанием. |
| Ионно-селективные электроды | Метод, основанный на измерении потенциала электрода, позволяет определить концентрацию ионов основания. |
| Спектроскопические методы | Анализ оснований с помощью измерения их поглощения, испускания или рассеяния электромагнитного излучения. |
| Гравиметрические методы | Определение содержания оснований путем измерения массы соединений, содержащих основания. |
Выбор метода определения основания зависит от его свойств, концентрации и требований анализа. Комбинированный подход и использование нескольких методов часто позволяют достичь наибольшей точности результатов.