Молекулы вещества - это основные строительные блоки всех материальных объектов, их "кирпичики". Согласно учебникам химии, молекулы обладают определенным количеством атомов, связанных между собой. Однако, существует ли какой-то непосредственный способ доказать их существование? Или это просто теория, выдвинутая научным сообществом?
На протяжении многих веков, ученые предлагали различные теории, объясняющие сущность молекул вещества. Одной из наиболее известных теорий является теория Авогадро, согласно которой молекулы состоят из атомов, связанных между собой определенным образом. Эта теория соответствует нашему современному представлению о строении вещества и подтверждается множеством экспериментальных данных.
Однако, доказательства существования молекул вещества не ограничиваются только теоретическими моделями и математическими расчетами. С помощью современных технологий и приборов, ученые смогли "увидеть" молекулы. Например, с помощью сканирующей туннельной микроскопии (СТМ) можно наблюдать отдельные атомы и молекулы на поверхности материалов.
Таким образом, существуют как теоретические, так и экспериментальные подходы к доказательству молекулярной структуры вещества. Оба эти способа подтверждают наличие молекул и позволяют понять их влияние на свойства вещества. Но все же, до последних времен невозможно было наблюдать или фотографировать молекулы вещества. Их существование было известно лишь по косвенным данным, получаемым с помощью химических реакций и физических свойств вещества.
Молекулярная теория вещества: история и разработка
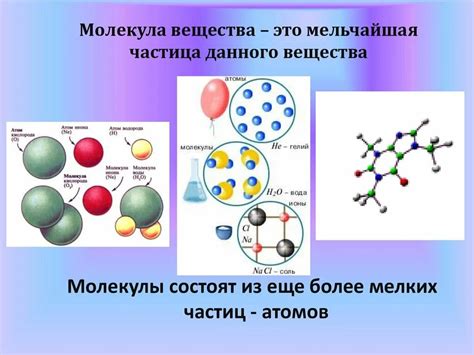
Идея о существовании молекул - мельчайших частиц вещества, состоящих из атомов, была впервые высказана древнегреческими философами и атомистами, такими как Демокрит и Эпикур. Однако, идея молекулярной структуры вещества официально признана и разработана только в XIX веке.
Предшественники молекулярной теории, такие ученые, как Роберт Бойль и Джон Далтон, внесли значительный вклад в формулировку основных принципов теории. Однако, сам термин "молекула" был введен лишь позже, в 1811 году, французским химиком Амедео Авогадро.
Одним из важнейших этапов в развитии молекулярной теории стало открытие Джона Джеймса Томсона в 1897 году электрона - частицы, которая является частью атомов и может двигаться вокруг ядра. Это новое открытие полностью изменило представление об атомной структуре вещества и позволило дальнейшему развитию молекулярной теории.
Современная молекулярная теория включает в себя такие ключевые элементы, как представление о молекулах, их размерах, форме и структуре. Теория также объясняет, как молекулы взаимодействуют между собой и какие силы действуют между ними. Благодаря молекулярной теории можно объяснить различные физические и химические явления, такие как тепловое движение, состояния вещества, химические реакции и многое другое.
Сегодня молекулярная теория является фундаментом для многих научных и технологических открытий. Она позволяет разрабатывать новые материалы, прогнозировать свойства вещества, создавать новые лекарства и изобретать новые способы производства энергии. Молекулярная теория вещества остается одной из самых актуальных и важных теорий в науке.
Экспериментальные доказательства существования молекул

Тем не менее, с развитием научных методик и технологий было проведено множество экспериментов, которые позволили ученым доказать наличие молекул и определить их основные свойства.
Одним из первых экспериментов, которые подтвердили существование молекул, был опыт с диффузией газов, проведенный Томасом Грэмом в 1829 году. Он обнаружил, что различные газы распространяются через полупроницаемую перегородку с различной скоростью, что говорило о том, что газы состоят из отдельных, неразрывных частиц - молекул.
Другим важным экспериментом, который подтвердил существование молекул, был опыт с растворами, проведенный Жаном Батистом Андре Маслейнсом в 1859 году. Он исследовал свойства различных растворов и обнаружил, что они могут иметь разные химические и физические свойства в зависимости от содержащихся в них молекул.
Современные методы науки позволяют более точно определить химический состав и структуру молекул. Например, методы спектроскопии позволяют исследовать спектральные характеристики молекул и определить их структуру.
Также, с использованием электронных микроскопов, ученым удалось визуально наблюдать отдельные молекулы и атомы, что стало окончательным доказательством их существования и структуры.
Таким образом, экспериментальные исследования и методы, разработанные учеными, позволяют подтвердить существование молекул вещества и изучать их свойства, что является основой для множества научных открытий и технологических применений.
Физические и химические свойства вещества, связанные с молекулярной структурой
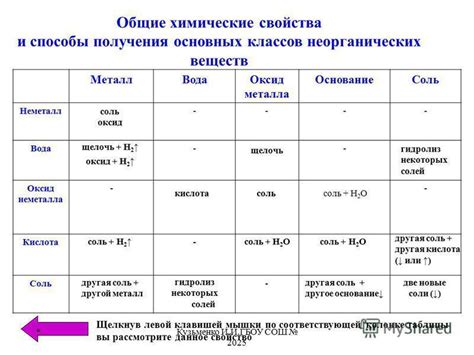
Молекулярная структура вещества определяет его физические и химические свойства. Молекулы вещества состоят из атомов, которые соединяются в определенном порядке и образуют различные структуры. Взаимное расположение атомов в молекуле и их тип влияют на многие свойства вещества.
Одно из основных физических свойств, зависящих от молекулярной структуры, - это плотность вещества. Структура молекул влияет на то, как тесно они упаковываются друг к другу. Например, вещества с простой молекулярной структурой, такие как газы, обычно имеют низкую плотность, потому что их молекулы отделены друг от друга большими промежутками. Наоборот, вещества с сложной молекулярной структурой, такие как металлы, могут иметь высокую плотность из-за тесной упаковки их атомов.
Свойства вещества также могут быть связаны с взаимодействием молекул между собой. Например, физические свойства, такие как температура плавления и кипения, зависят от сил притяжения между молекулами. Чем сильнее эти притяжительные силы, тем выше температура плавления и кипения вещества. Для веществ с простой молекулярной структурой такие силы обычно слабы, поэтому их температуры плавления и кипения невысоки. Вещества с более сложной молекулярной структурой, такие как полимеры, могут образовывать сильные взаимодействия между молекулами и иметь более высокие температуры плавления и кипения.
Химические свойства вещества также могут быть связаны с его молекулярной структурой. Например, тип связей между атомами в молекуле определяет химическую реактивность вещества. Вещества с простой молекулярной структурой, такие как газы, обычно мало реактивны. Наоборот, вещества с более сложной молекулярной структурой, такие как органические соединения, обычно проявляют большую химическую активность.
Молекулярная структура вещества играет ключевую роль во многих физических и химических свойствах. Понимание этой структуры помогает ученым объяснять и предсказывать поведение вещества, а также разрабатывать новые материалы с желаемыми свойствами.
Альтернативные подходы к пониманию состава вещества

На протяжении многих веков ученые исследовали состав вещества и разрабатывали различные теории о его структуре. Однако, наряду с классическими подходами, были также предложены альтернативные модели, которые позволяют понять состав вещества с других точек зрения.
Одним из таких подходов является теория квантовых полей, которая опирается на принципы квантовой механики. Согласно этой теории, вещество состоит из элементарных частиц, таких как кварки, лептоны и бозоны. Квантовые поля описывают взаимодействия этих частиц и позволяют объяснить различные феномены, происходящие на микроуровне.
Другим подходом является модель структуры вещества, основанная на представлении о молекулярном строении. Согласно этой модели, вещество состоит из молекул, которые объединяются в кристаллическую решетку или образуют жидкую или газообразную среду. Молекулы могут быть разных типов и соединяться различными способами, что определяет их химические и физические свойства.
Также существуют идеи о том, что состав вещества может быть связан с его энергетическим состоянием. Например, в рамках теории струн предполагается, что микроскопические объекты вещества могут быть представлены как колеблющиеся струны, которые имеют различные физические свойства в зависимости от своей формы и взаимодействий.