Химия является одной из ключевых наук, изучающей строение и свойства вещества. Одним из основных строительных блоков атома являются электрически заряженные частицы - протоны и электроны. Несмотря на то, что оба они являются элементами атома, у них есть существенные различия, которые делают их уникальными.
Протон, как и электрон, является элементарной частицей, однако его заряд положительный. Протон находится в ядре атома вместе с нейтронами, и его количество определяет проинициализированную структуру атома. Масса протона равна единице по отношению к массе электрона, и это делает его гораздо более массивным.
Электрон, в отличие от протона, обладает отрицательным зарядом. Он находится вокруг ядра атома, заполняя электронные оболочки. Масса электрона много меньше массы протона и составляет около 1/1836 его массы. Электроны являются ключевыми участниками в химических реакциях и обладают электромагнитной природой.
Структура и свойства протона и электрона в химии
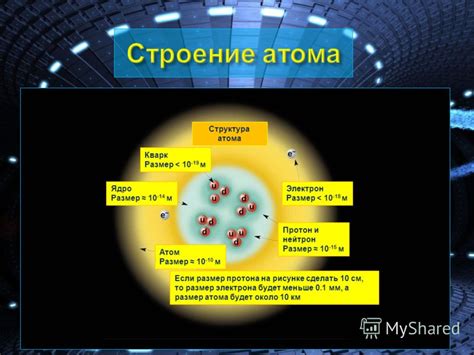
Протон является положительно заряженной частицей, которая находится внутри ядра атома. Он имеет относительно большую массу и обозначается символом "p". Протон состоит из кварков, элементарных частиц, которые являются строительными блоками протона и других частиц.
Электрон, в отличие от протона, имеет отрицательный заряд и находится вокруг ядра атома. Он обладает очень малой массой по сравнению с протоном и обозначается символом "e". Электрон не содержит кварков, и считается фундаментальной частицей, то есть не может быть разделена на более мелкие компоненты.
У протона и электрона есть еще одно важное свойство - их заряд. Протон имеет положительный заряд, равный элементарному заряду, который обозначается символом "e+". Электрон имеет отрицательный заряд, равный по модулю значению элементарного заряда, и обозначается символом "e-".
Структура и свойства протона и электрона определяют их роль в химических реакциях. Протоны, являясь частью ядра атома, определяют его химические и физические свойства, такие как масса и атомный номер. Электроны, находясь внутри области вокруг ядра, определяют химические свойства атома, такие как его реакционная способность и возможность формирования связей с другими атомами.
Таким образом, протон и электрон взаимодействуют в химических реакциях, образуя химические связи и определяя свойства вещества. Их различия в структуре и заряде делают их важными составляющими атома и основными участниками химических процессов.
Масса и заряд протона
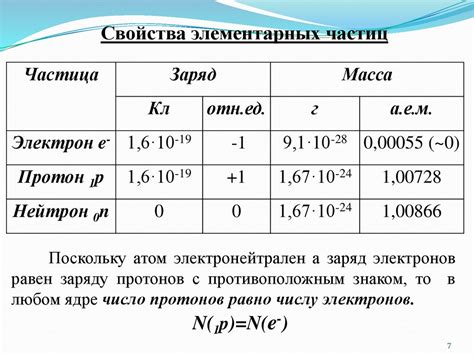
Масса протона составляет примерно 1,673·10-27 кг, что делает его примерно 1836 раз тяжелее электрона. Он является субатомной частицей, входящей в состав атомного ядра вместе с нейтронами, которые также имеют массу приблизительно равную массе протона.
Заряд протона составляет положительный элементарный заряд, равный 1,602·10-19 Кл. Это делает протон положительно заряженной частицей, в то время как электрон, наоборот, является отрицательно заряженной частицей.
Протон играет важную роль в определении химических свойств атомов и молекул, так как их зарядовый баланс определяется числом протонов и электронов внутри атомов.
Знание о массе и заряде протона позволяет ученым строить модели атомов и понимать процессы, происходящие на молекулярном уровне, что является основой для понимания множества химических явлений и реакций.
Масса и заряд электрона
Масса электрона составляет примерно 9,1 · 10^-31 кг (колеблется также в зависимости от релятивистских эффектов). Она очень мала по сравнению с массой протона и нейтрона, формирующих ядро атома.
Электроны играют ключевую роль в химических реакциях и электронных структурах атомов и молекул. Их движение вокруг атомного ядра обуславлиет электронную оболочку, которая определяет химические свойства элемента и его способность вступать в химические соединения.
Местоположение протона в атоме
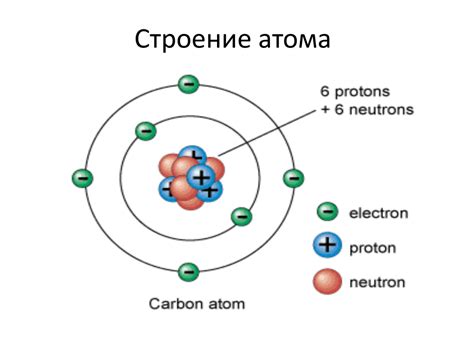
Протоны находятся в нейтральных ионных атомах в атомном ядре вместе с нейтронами. Ядро атома состоит из протонов и нейтронов, в то время как электроны находятся в области вокруг ядра, на энергетических уровнях.
Местоположение протона в атоме положительно заряженного. Он находится в центральной части атома - атомном ядре. Протоны не перемещаются внутри атома и находятся на месте.
Протон имеет массу, сравнимую с нейтронами, но гораздо большую, чем у электронов. Он также взаимодействует с другими частицами через электромагнитные силы и участвует в образовании химических соединений и реакциях.
Наличие протонов в атоме определяет его химические свойства, так как они являются носителями положительного заряда и взаимодействуют с электронами, образуя электростатические силы. Местоположение протона в атоме объясняет его роль в процессах химической связи и структуре вещества.
Местоположение электрона в атоме
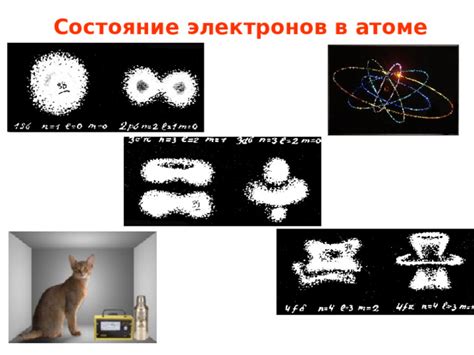
Согласно модели Шредингера, электрон распределен вокруг ядра в форме электронных облаков или орбиталей. Орбитали представляют собой вероятностные области, в которых можно найти электрон с определенной вероятностью.
Местоположение электрона в атоме можно определить с помощью квантовых чисел, таких как главное квантовое число, орбитальное квантовое число и магнитное квантовое число. Главное квантовое число определяет энергетический уровень электрона, орбитальное квантовое число указывает на форму орбитали, а магнитное квантовое число определяет ориентацию орбитали в пространстве.
Таким образом, местоположение электрона в атоме не является точным и фиксированным, а представляет собой определенные вероятностные области. Это объясняет феномены химической связи, реакций и спектроскопии, связанные с движением электронов в атоме.
Взаимодействия протона и электрона с другими частицами

Протон, как положительно заряженная частица, обладает способностью притягивать отрицательно заряженные электроны соседних атомов, что создает связь между атомами и формирует молекулы. Этот тип притяжения называется кулоновским притяжением и является одним из основных факторов, определяющих химические связи между атомами в молекулах.
Электроны, в свою очередь, обладают отрицательным электрическим зарядом и могут взаимодействовать с другими атомами и молекулами, а также с положительно заряженными ионами. Они могут быть переданы с одной молекулы на другую, что приводит к образованию различных реакций.
Взаимодействия протона и электрона с другими частицами определяют химические свойства вещества и позволяют проводить различные химические реакции, такие как окислительно-восстановительные реакции, образование химических связей и разрушение молекул.
Изучение взаимодействия протона и электрона является одной из основных задач химии и открывает возможности для создания новых материалов и прогресса в различных областях научных исследований.
Роль протона и электрона в химических реакциях
Во время химических реакций, протоны и электроны могут переходить из одной молекулы в другую, образуя новые связи и разрывая старые. Протоны могут быть переданы от одного атома к другому, изменяя степень окисления атомов и создавая ионы. Электроны, в свою очередь, могут быть перенесены между атомами, что приводит к образованию новых химических связей и образованию или разрушению молекул.
Протоны могут также участвовать в кислотно-основных реакциях, где они сопровождаются передачей водородных ионов. Электроны же могут служить основой для различных видов реакций, таких как окислительно-восстановительные реакции, где происходит передача электронов между веществами.
Роль протона и электрона в химических реакциях зависит от их электрических свойств и способности образовывать связи с другими атомами. Благодаря этим свойствам, протоны и электроны позволяют атомам взаимодействовать друг с другом и образовывать новые вещества.
| Свойство | Протон | Электрон |
|---|---|---|
| Масса | Относительно большая (примерно 1 атомная единица массы) | Относительно малая (примерно 1/1836 атомной единицы массы) |
| Заряд | Положительный (+1) | Отрицательный (-1) |
| Местоположение | В ядре атома | Вокруг ядра в электронных оболочках |