Ортофосфорная и фосфорная кислоты - два основных типа соединений, которые содержат фосфор. И хотя они имеют общую основу, они имеют некоторые значительные различия, которые важно понимать.
Фосфорная кислота - это общий термин, который относится к различным соединениям, содержащим фосфор. Она может быть простым соединением P2O5 или многократным соединением, таким как H3PO4, но обычно наиболее распространена фосфорная кислота как ортофосфорная кислота.
Ортофосфорная кислота (H3PO4) - самая распространенная форма фосфорной кислоты и широко используется в промышленности и сельском хозяйстве. Она имеет три протонных группы, что делает ее трехосновной кислотой. Ортофосфорная кислота используется в процессе производства минеральных удобрений, а также в пищевой промышленности для регулирования уровня pH продуктов.
Ортофосфорная и фосфорная кислота: основные отличия

Ортофосфорная кислота:
Ортофосфорная кислота (H3PO4) – это трехосновная кислота, состоящая из молекулы фосфорной кислоты с тремя присоединенными протонами. Она также известна под названием фосфорной(V) кислоты.
Фосфорная кислота:
Фосфорная кислота (H3PO3) – это двухосновная кислота, состоящая из молекулы фосфитной кислоты с двумя присоединенными протонами. Она также известна под названием фосфорной(III) кислоты.
Отличия:
- Количество присоединенных протонов: ортофосфорная кислота имеет 3 протона, в то время как фосфорная кислота имеет только 2 протона.
- Структура: ортофосфорная кислота образована молекулами фосфорной кислоты, в которой все 3 протона присоединены к атомам кислорода. В то же время, фосфорная кислота состоит из молекулы фосфитной кислоты, в которой только 2 протона присоединены к атомам кислорода.
- Окислительность: ортофосфорная кислота является сильным оксидантом, в то время как фосфорная кислота является слабым окислителем.
- Применение: ортофосфорная кислота используется в различных областях, включая производство удобрений, пищевую промышленность и металлургию. Фосфорная кислота находит применение в производстве пластиков, полимеров и стимуляторов роста растений.
Ортофосфорная и фосфорная кислота имеют различные свойства и применение. Изучение их химической структуры и особенностей помогает понять их различия в реакционной способности и влиянии на окружающую среду.
Ортофосфорная кислота и ее свойства

Во-первых, ортофосфорная кислота является трипротической кислотой, то есть каждая молекула кислоты может отдать три протона. Это делает ее более кислотной, чем фосфорная кислота, которая является двухпротической.
Во-вторых, ортофосфорная кислота обладает различными физическими свойствами. Она является бесцветной и прозрачной жидкостью с характерным запахом. Она хорошо растворима в воде и образует щелочную среду.
Ортофосфорная кислота обладает высокой адсорбционной способностью, способствуя удержанию влаги во многих материалах. Она также может быть использована в качестве катализатора или компонента в процессах синтеза органических соединений.
Эта кислота также является сильным окислителем, что делает ее полезной при некоторых химических реакциях. Ее использование может быть опасным из-за ее коррозивных свойств и высокой токсичности.
Ортофосфорная кислота имеет широкий спектр применения в различных отраслях, включая пищевую промышленность, медицину, сельское хозяйство и производство удобрений. Это важное химическое соединение, играющее ключевую роль во многих процессах и применениях.
Фосфорная кислота и ее особенности

Фосфорная кислота имеет структуру смежных кислородных атомов в виде цепи, в которой присутствуют промежуточные кислородные атомы. Это отличает ее от ортофосфорной кислоты, которая имеет структуру с трехвалентным фосфором, окруженным четырьмя кислородными атомами.
Фосфорная кислота является сильным кислотным соединением и часто используется в различных отраслях промышленности. Она обладает высокой растворимостью в воде и образует густой сиропообразный раствор.
Эта кислота обладает свойствами окислителя и дезинфицирующего средства. Она может применяться в производстве удобрений, пищевой промышленности, фармацевтике и других областях.
Важно отметить, что фосфорная кислота является химически активным соединением и требует особой осторожности при обращении с ней. Работа с ней должна проводиться в соответствии с правилами безопасности и специальным оборудованием.
Кислотность ищется и измеряется разными способами

Ортофосфорная кислота (H3PO4) обладает высокой кислотностью и широко используется в различных промышленных и лабораторных процессах. Ее кислотность может быть измерена посредством рН-метра или индикаторной бумажкой. Когда ортофосфорная кислота диссоциирует в воде, она образует три протонных иона (H+), что делает ее сильной кислотой.
Фосфорная кислота (H3PO3) обладает более слабой кислотностью по сравнению с ортофосфорной. Она также может быть измерена с помощью рН-метра или индикаторной бумажкой. Фосфорная кислота диссоциирует в воде, образуя два протонных иона (H+), что делает ее слабой кислотой.
Ортофосфорная кислота и фосфорная кислота имеют различные применения в разных отраслях науки и промышленности, и понимание их различий в кислотности является ключевым для правильного использования.
Примечание: важно помнить, что при работе с кислотами необходимо соблюдать меры предосторожности и использовать личную защиту, так как они могут быть опасными для здоровья и окружающей среды.
Структурные различия между ортофосфорной и фосфорной кислотой
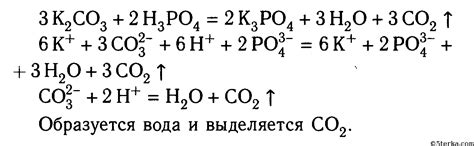
| Ортофосфорная кислота | Фосфорная кислота |
|---|---|
 |  |
| Молекула ортофосфорной кислоты содержит три атома водорода | Молекула фосфорной кислоты содержит три остатка гидроксильной группы (-OH) |
| Общая формула: H3PO4 | Общая формула: H3PO3 |
Ортофосфорная кислота имеет более сложную структуру, состоящую из молекулы фосфорной кислоты, в которой все три атома водорода замещены остатками гидроксильной группы.
Фосфорная кислота, с другой стороны, имеет молекулу, в которой есть только один остаток гидроксильной группы, а два атома водорода остаются незамещенными.
Эти структурные различия влияют на свойства и реакционную способность этих двух кислот. Ортофосфорная кислота является более сильной кислотой и может образовывать более стабильные соединения, чем фосфорная кислота.
Реакции ортофосфорной и фосфорной кислоты с другими веществами
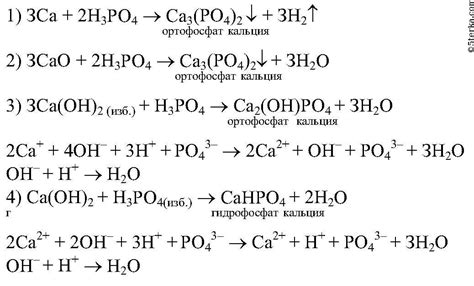
Ортофосфорная и фосфорная кислоты обладают различными свойствами и способностью вступать в реакции с другими веществами. Вот некоторые из них:
Реакции ортофосфорной кислоты
1. Образование фосфорных солей – ортофосфорная кислота обладает выраженной кислотностью и может реагировать с основаниями, образуя соли. Например, реакция с гидроксидом натрия приводит к образованию натрия ортофосфата:
- H3PO4 + 3NaOH → Na3PO4 + 3H2O
2. Нейтрализация – ортофосфорная кислота может реагировать с щелочами, образуя соли и воду:
- H3PO4 + 3KOH → K3PO4 + 3H2O
3. Образование эстеров – ортофосфорная кислота может реагировать с спиртами, образуя эстеры. Например, реакция с метанолом приводит к образованию метилортофосфорной кислоты:
- H3PO4 + 3CH3OH → (CH3)3PO4 + 3H2O
Реакции фосфорной кислоты
1. Дезгидратация – фосфорная кислота может дезгидрироваться при нагревании, образуя фосфаты:
- 2H3PO4 → H4P2O7 + H2O
2. Образование кислотных солей – фосфорная кислота может образовывать кислотные соли с некоторыми металлами, например:
- 3H3PO4 + 4Al(OH)3 → Al(H2PO4)3 + 3H2O
3. Реакция с карбонатами – фосфорная кислота может реагировать с карбонатами, образуя соль карбоната металла и углекислый газ:
- 2H3PO4 + 3CaCO3 → Ca3(PO4)2 + 3CO2 + 3H2O
Такие реакции с другими веществами позволяют использовать ортофосфорную и фосфорную кислоты в различных технических, химических и пищевых процессах.
Применение ортофосфорной и фосфорной кислоты в разных областях

Ортофосфорная кислота (H3PO4) широко используется в химической промышленности, производстве пищевых добавок, сельском хозяйстве и медицине. В химической промышленности ортофосфорная кислота используется в качестве окислителя, регулятора pH и компонента при производстве удобрений, фосфатных солей и красителей. Также, она используется в качестве добавки в пищу для регулирования кислотности и антиоксиданта.
Фосфорная кислота (H3PO3) также находит применение в химической промышленности, а также в производстве удобрений и фармацевтической промышленности. Она используется для синтеза фосфитов, промывки металлических поверхностей перед окрашиванием и в качестве антиоксиданта. Фосфорная кислота также применяется в медицине, например, для обработки ран и регулирования pH в некоторых медицинских препаратах.
Обе эти кислоты имеют важное значение в сельском хозяйстве, так как являются основными источниками фосфора, необходимого растениям для нормального роста и развития. Они используются в виде удобрений, подкормок и добавок, чтобы обеспечить растениям достаточное количество фосфора. Фосфор особенно важен для развития корневой системы, цветения, созревания плодов и улучшения качества урожая.
Важно отметить, что ортофосфорная и фосфорная кислоты являются химическими веществами и могут быть опасными, поэтому их использование должно осуществляться соответствующим образом и в соответствии с рекомендациями безопасности.
Влияние ортофосфорной и фосфорной кислоты на окружающую среду

Одной из основных проблем, связанных с использованием ортофосфорной и фосфорной кислот, является их потенциальный выход в окружающую среду в результате несанкционированного сброса или утечки. При попадании в водные ресурсы эти кислоты могут вызывать загрязнение воды и негативно влиять на деликатный баланс экосистем.
Ортофосфорная и фосфорная кислоты могут вызывать кислотные осадки и изменять pH воды. Это может привести к снижению разнообразия и численности рыб и других водных организмов, а также к разрушению их гнездовий и местообитаний.
Кроме того, ортофосфорная и фосфорная кислоты могут быть опасными для человеческого здоровья при длительном воздействии или больших концентрациях. Пары этих кислот могут раздражать дыхательные пути, вызывать ожоги кожи и глаз, а также иметь токсические свойства.
Следовательно, важно строго контролировать использование ортофосфорной и фосфорной кислот, а также принимать меры по предотвращению и ликвидации возможных аварийных ситуаций. Правильное хранение, транспортировка и утилизация этих веществ позволят минимизировать негативное влияние на окружающую среду и обеспечить безопасность людей и животных, а также сохранить экологическое равновесие.
| Основные последствия использования ортофосфорной и фосфорной кислот: | Возможные меры предотвращения и ликвидации |
|---|---|
| Загрязнение воды и нарушение экосистем | Строгий контроль сброса и утечек, применение защитных мер |
| Снижение разнообразия и численности водных организмов | Мониторинг водных ресурсов, регулирование использования кислот |
| Опасность для здоровья человека | Обучение персонала, соблюдение правил безопасности, использование защитной экипировки |



