Взаимодействие молекул является основной составляющей процессов, происходящих в физической химии и физике твердого тела. Это явление описывает взаимное воздействие атомов и молекул друг на друга, определяя свойства веществ и их поведение. В физике существуют различные типы взаимодействия молекул, каждое из которых имеет свои особенности и проявления.
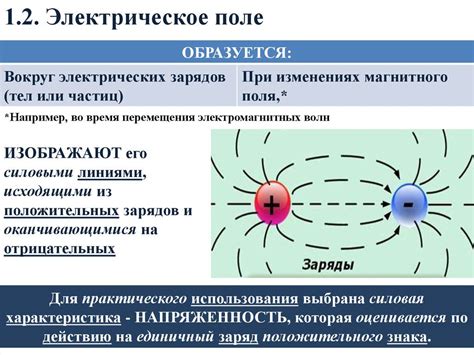
Одним из основных понятий взаимодействия молекул является электростатическое взаимодействие. Оно возникает в результате действия притяжения или отталкивания электрических зарядов, обусловленных наличием электронов и ионов. Электростатическое взаимодействие молекул влияет на химическую связь, силу поверхностного натяжения, свойства расплавов и незаметное для нас притяжение молекул в быту.
Ван-дер-Ваальсовы силы являются еще одним типом взаимодействия молекул. Они возникают за счет неравномерного распределения электрического заряда в молекуле, что приводит к временному возникновению диполя. Это взаимодействие может быть как притягивающим, так и отталкивающим, и оно играет важную роль в свойствах газов, жидкостей и твердых тел, определяя, например, их тепловое расширение или эластичность.
Гидродинамическое взаимодействие молекул определяет поведение жидкостей и газов и связано с их движением. Это взаимодействие образует сложные потоки, вихри и течения, которые существенно влияют на физические процессы в природный и технических объектах. Гидродинамическое взаимодействие молекул также определяет физические свойства жидкостей и газов, такие как вязкость, плотность и давление.
Изучение взаимодействия молекул является важной составляющей физической химии и физики твердого тела, позволяющей понять основные принципы и законы, которыми руководствуется весь микромир. Знание основ взаимодействия молекул дает возможность создавать новые материалы с определенными свойствами, улучшать технологические процессы и разрабатывать новые методы анализа вещества.
Электростатическое взаимодействие молекул: объяснение и примеры
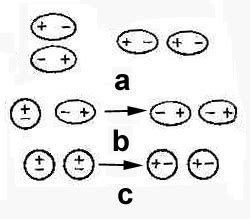
Электростатическое взаимодействие играет важную роль во многих процессах и явлениях в физике, химии и биологии. В химических реакциях, например, заряды молекул влияют на силу притяжения или отталкивания между ними, что в конечном счете определяет их соединение или разрушение. В биологических системах электростатическое взаимодействие молекул, таких как белки, может регулировать их структуру и функцию.
Примером электростатического взаимодействия молекул является сила притяжения между положительно и отрицательно заряженными ионами. Например, в молекуле соли натрия (NaCl) положительно заряженные натриевые ионы и отрицательно заряженные хлоридные ионы притягиваются друг к другу, образуя кристаллическую решетку. Это взаимодействие обусловливает свойства и характеристики солей, такие как их растворимость и температурные свойства.
Еще одним примером является силовое поле вокруг заряженного тела. Если приблизить к нему нейтральный предмет, такой как шарик из фольги или волосок, то произойдет притяжение или отталкивание, обусловленное электростатическим взаимодействием между заряженным телом и зарядами, присутствующими в нейтральном предмете.
Электростатическое взаимодействие молекул является основой для понимания многих явлений и процессов, происходящих в мире вокруг нас. Изучение этой силы позволяет нам лучше понять и объяснить поведение материи и ее взаимодействие в различных областях науки.
Ван-дер-Ваальсово взаимодействие молекул: суть и проявления
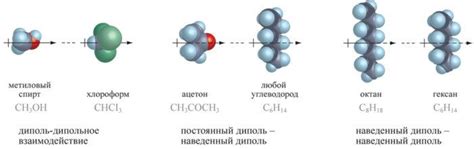
Основной причиной ван-дер-Ваальсового взаимодействия являются электрические поля, создаваемые электронами вокруг атомов. Когда две молекулы находятся близко друг к другу, появляется диполь-дипольное взаимодействие между их электрическими полями.
Проявление ван-дер-Ваальсового взаимодействия можно наблюдать в различных физических явлениях. Например, ван-дер-Ваальсовы силы приводят к сжатию газов в жидкость при низких температурах и высоких давлениях. Это объясняется тем, что молекулы газа приближаются друг к другу, образуя слабую связь между собой.
Еще одним проявлением ван-дер-Ваальсового взаимодействия является сила адгезии, которая позволяет молекулам клеиться друг к другу. Это явление особенно важно для свойств поверхности жидкостей и твердых тел. Например, благодаря ван-дер-Ваальсовому взаимодействию вода может образовывать капли и мокнуть поверхность.
Ван-дер-Ваальсовое взаимодействие также играет важную роль в свойствах межмолекулярных взаимодействий веществ. Например, оно может влиять на температуру кипения и плавления веществ, а также на их плотность и вязкость.
Гидродинамическое взаимодействие молекул: основные принципы
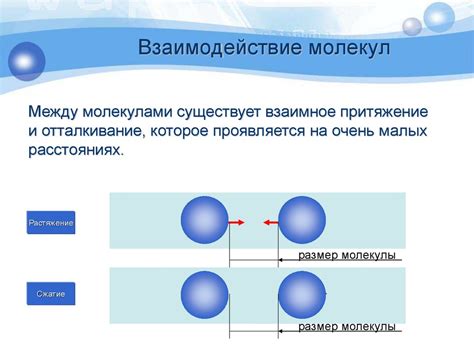
Основные принципы гидродинамического взаимодействия молекул в физике включают:
- Равновесное состояние: В равновесном состоянии молекулы жидкости или газа распределены равномерно и не испытывают взаимное взаимодействие.
- Давление: Гидродинамическое взаимодействие молекул приводит к возникновению давления. Давление определяется силой, с которой молекулы сталкиваются друг с другом.
- Вязкость: Вязкость определяет способность жидкости сопротивляться деформации и зависит от взаимодействия молекул.
- Поток: Взаимодействие молекул в жидкости или газе приводит к образованию потока, то есть к движению молекул в определенном направлении.
Примером гидродинамического взаимодействия молекул является течение воды в реке. Молекулы воды взаимодействуют друг с другом, образуют поток и создают давление на препятствия, такие как камни или берега.
Изучение гидродинамического взаимодействия молекул является важным для понимания различных физических явлений, таких как движение жидкостей и газов, течение рек и океанов, а также для разработки различных технологий, связанных с гидравликой и аэродинамикой.
Магнитное взаимодействие молекул: виды и приложения
Существует несколько видов магнитного взаимодействия молекул, включая диполь-дипольное взаимодействие, обменное взаимодействие и интеракцию с внешним магнитным полем.
Диполь-дипольное взаимодействие возникает между двумя молекулами, у которых есть магнитные диполи. Магнитные диполи образуются благодаря наличию неравномерно распределенных зарядов или намагниченных атомных ядер внутри молекулы. Это взаимодействие может быть как притяжением, так и отталкиванием, в зависимости от ориентации диполей.
Обменное взаимодействие возникает между молекулами, содержащими неспаренные электроны. Это взаимодействие основано на обмене энергией между молекулами и может приводить к появлению сильного магнитного поля.
Внешние магнитные поля также могут влиять на молекулярные магнитные свойства. Магнитное поле может изменять ориентацию магнитных диполей в молекулах, что приводит к изменению их магнитных свойств.
Магнитное взаимодействие молекул имеет широкое применение в различных областях. Например, в медицине оно используется для создания магнитно-резонансных изображений (МРТ), которые позволяют получить детальную информацию о структуре тканей и органов человека. В электронике и магнитных устройствах магнитное взаимодействие молекул играет важную роль в создании магнитных памяти и твердотельных магнитных датчиков. В химии магнитное взаимодействие молекул используется для изучения структуры и свойств различных химических соединений.
Ядерное взаимодействие молекул: механизмы и процессы
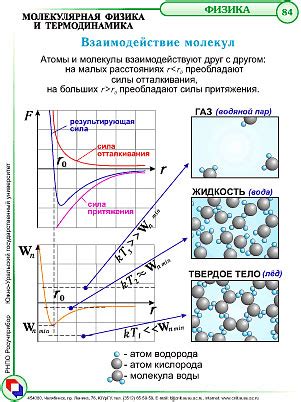
Ядерное взаимодействие молекул может происходить различными способами. Одним из основных механизмов является ядерный обмен, когда ядра молекул обмениваются протонами и нейтронами. Это может приводить к изменению структуры и свойств молекулы, а также к возникновению новых частиц и изотопов. Ядерный обмен может происходить в результате столкновения молекул с другими молекулами, а также под воздействием внешних факторов, таких как высокая энергия или радиоактивное излучение.
Еще одним механизмом ядерного взаимодействия молекул является ядерный резонанс. Этот процесс происходит при определенных условиях, когда внешнее воздействие вызывает резонансное взаимодействие ядерных частиц. В результате этого могут возникать колебания и переходы между различными энергетическими состояниями молекулы. Ядерный резонанс используется, например, в ядерном магнитном резонансе (ЯМР) для изучения строения и свойств молекул.
Также в ядерном взаимодействии молекул можно выделить процессы ядерного замедления и ядерного распада. При ядерном замедлении быстрые ядра могут взаимодействовать с окружающими молекулами и передавать им часть своей энергии и импульса. Это происходит, например, в результате столкновений атомов в газе при высоких температурах. Ядерный распад, в свою очередь, представляет собой процесс перехода нестабильных ядер в более устойчивые состояния или в другие ядра с меньшим количеством протонов и нейтронов. Ядерный распад может быть спонтанным или индуцированным различными внешними воздействиями.
| Механизм | Описание | Примеры |
|---|---|---|
| Ядерный обмен | Обмен протонами и нейтронами между ядрами молекулы | Реакции ядерного синтеза в звездах |
| Ядерный резонанс | Резонансное взаимодействие ядер, вызывающее колебания молекулы | Ядерный магнитный резонанс (ЯМР) в спектроскопии |
| Ядерное замедление | Передача энергии и импульса быстрых ядер молекулам | Тепловые реакции в атомных реакторах |
| Ядерный распад | Переход нестабильных ядер в более устойчивые состояния | Радиоактивный распад в природе и в лабораторных условиях |
Таким образом, ядерное взаимодействие молекул играет важную роль во многих процессах и явлениях физики и химии. Оно позволяет понять основные механизмы взаимодействия молекул и ядерных частиц, а также исследовать свойства и структуру различных веществ.
Термическое взаимодействие молекул: теория и примеры
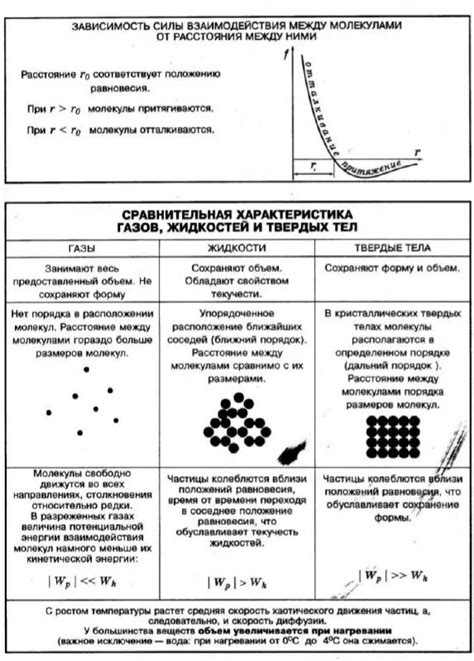
В физике существует такое понятие, как термическое взаимодействие молекул, которое описывает процессы переноса энергии и изменения физического состояния вещества при воздействии тепла. Тепловые явления играют важную роль во многих физических процессах, начиная от теплопроводности в твердых телах и заканчивая фазовыми переходами в жидкостях и газах.
Термическое взаимодействие молекул может быть объяснено на основе кинетической теории газов. Согласно этой теории, молекулы вещества постоянно движутся и сталкиваются друг с другом. В результате столкновений происходит перенос кинетической энергии от более быстрых молекул к более медленным, что приводит к повышению температуры вещества.
Примером термического взаимодействия молекул является теплопроводность. При нагревании одной частицы вещества, энергия переходит к соседним молекулам путем столкновений. Таким образом, тепло распространяется по всему объему вещества. Этот процесс можно наблюдать, например, при нагревании одного конца металлической палочки: тепло быстро распространяется по всей палочке, так как молекулы передают энергию через свои столкновения.
Другим примером является плавление льда. При повышении температуры лед постепенно переходит в состояние воды. Это происходит из-за термического взаимодействия молекул: энергия, поступающая на поверхность льда, вызывает возросшую активность его молекул, что приводит к разрыву водородных связей между молекулами и образованию жидкой воды.
Термическое взаимодействие молекул является фундаментальным понятием в физике и играет важную роль в объяснении различных физических процессов. Понимание этого взаимодействия позволяет лучше понять поведение вещества при разных температурах и применить это знание в решении практических задач.
Фотохимическое взаимодействие молекул: реакции и применение

Фотохимическое взаимодействие молекул основано на взаимодействии фотонов с молекулами вещества. Фотохимические реакции протекают под воздействием электромагнитного излучения определенной длины волны. В результате фотохимической реакции молекулы могут изменять свою структуру или происходить образование новых веществ.
Применение фотохимического взаимодействия молекул широко используется в различных областях науки и техники, таких как:
| Область применения | Примеры |
|---|---|
| Фотохимия | Фотосинтез, фотодеградация, фотополимеризация |
| Фотоэлектрохимия | Фотоэлектрические ячейки, фотокатализ |
| Медицина | Фотодинамическая терапия, фотосенсибилизация |
| Фотохромизм | Фотохромные материалы, оптические покрытия |
| Фотоизмерения | Фотоспектроскопия, фотоакустическая спектроскопия |
Фотохимические реакции имеют огромное значение в практических приложениях, от разработки новых материалов до лечения заболеваний. В изучении взаимодействия молекул в фотохимических реакциях используются методы фотоэлектрохимического исследования, фотохроматической спектроскопии, а также фотохимических реакций в трехфазных системах.