Конденсация – это процесс, при котором газовое вещество превращается в жидкость. Этот физический процесс основан на изменении внутренней энергии вещества. Когда температура газа понижается до определенного значения, его молекулы начинают сближаться и притягиваться друг к другу, формируя жидкость.
Внутренняя энергия – это сумма кинетической и потенциальной энергии всех частиц вещества. Во время конденсации газа, энергия переходит от кинетической формы (движение молекул) к потенциальной (силы притяжения между молекулами). Этот процесс приводит к снижению температуры и увеличению плотности вещества.
Когда молекулы газа конденсируются, они теряют кинетическую энергию, которая приводила их в движение. Из-за этого происходит охлаждение окружающей среды, так как энергия передается ей. С другой стороны, молекулы жидкости приобретают потенциальную энергию в результате притяжения друг к другу. Это приводит к увеличению внутренней энергии жидкости.
Внутренняя энергия и ее изменения при конденсации
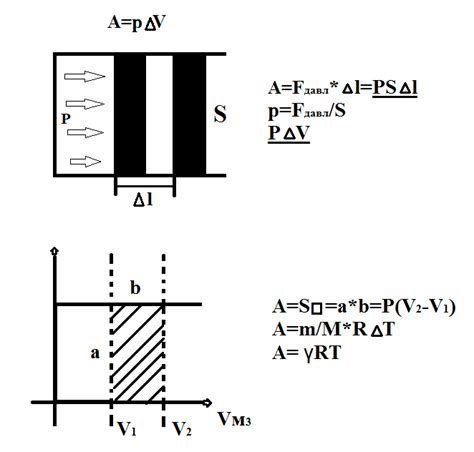
Сначала, при охлаждении газообразного вещества, его молекулы замедляют свое движение, что приводит к снижению их кинетической энергии. Это приводит к уменьшению внутренней энергии системы.
Когда вещество достигает своей температуры конденсации, происходит образование жидкой или твердой фазы. В этот момент молекулы вещества начинают образовывать упорядоченную структуру. Это вызывает изменение энергии взаимодействия между молекулами и приводит к изменению внутренней энергии системы.
Конденсация вещества сопровождается увеличением его внутренней энергии, так как образование более компактной фазы вызывает увеличение энергии межмолекулярных взаимодействий. Это приводит к тому, что конденсация вещества обычно сопровождается выделением тепла.
Таким образом, при конденсации происходят изменения внутренней энергии системы, связанные с изменением кинетической энергии молекул и изменением энергии взаимодействий между ними. Эти изменения внутренней энергии являются фундаментальными для понимания процессов конденсации и являются основой для объяснения тепловых эффектов, связанных с этим процессом.
Что такое внутренняя энергия?

Кинетическая энергия отвечает за движение частиц внутри системы. Она пропорциональна температуре вещества и зависит от его скорости. Кинетическая энергия может быть в форме тепла, если энергия передается между системами, или в форме работы, если энергия используется для перемещения или противодействия внешним силам.
Потенциальная энергия отвечает за силы внутри системы, которые связаны с взаимодействием между частицами. Она зависит от расстояния между частицами и силы притяжения или отталкивания между ними. Потенциальная энергия может быть в форме энергии связи, если частицы в системе взаимодействуют через химические или ядерные связи.
Всякий раз, когда происходит физический или химический процесс, внутренняя энергия системы может изменяться. Например, при конденсации, когда газ переходит в жидкость, внутренняя энергия уменьшается, так как в процессе конденсации энергия выделяется в виде тепла. Это можно объяснить тем, что при переходе вещества из газообразного состояния в жидкое, частицы молекул образуют более упорядоченную структуру, что приводит к снижению их кинетической энергии.
Принцип сохранения энергии

Конденсация - это процесс перехода вещества из газообразного состояния в жидкое при снижении температуры. Во время конденсации происходит освобождение энергии в виде тепла, которая была затрачена на разделение частиц газа и сжатие его в жидкость. Таким образом, внутренняя энергия системы при конденсации уменьшается, но сохраняется в виде тепла.
Это объясняется тем, что при конденсации происходит уплотнение частиц газа, образуя жидкость. Уплотнение сопровождается силами взаимодействия между молекулами, которые приводят к увеличению потенциальной энергии системы. При этом кинетическая энергия молекул уменьшается, так как их скорость снижается. Однако, общая сумма кинетической и потенциальной энергии остается постоянной.
Таким образом, принцип сохранения энергии подтверждается при конденсации, где потеря кинетической энергии компенсируется увеличением потенциальной энергии системы. Важно отметить, что эта энергия может быть использована в дальнейшем при других физических процессах.
Конденсация и ее процессы

Внутренняя энергия вещества - это сумма кинетической и потенциальной энергии его молекул. В газообразном состоянии молекулы движутся быстро и хаотично, что приводит к высокой кинетической энергии. При конденсации молекулы замедляют свое движение и становятся ближе друг к другу, что приводит к увеличению потенциальной энергии.
Внутренняя энергия вещества сохраняется при конденсации, однако ее форма изменяется. Увеличение потенциальной энергии сопровождается уменьшением кинетической энергии молекул. Результатом этого процесса является выделение тепла, которое поглощается окружающей средой.
Конденсация может происходить при снижении температуры газа или при увеличении давления. После конденсации вещество образует жидкую фазу, в которой молекулы могут сохранять свою близость друг к другу и взаимодействовать с соседними молекулами.
Важно отметить, что конденсационная теплота, освобождающаяся при конденсации, играет важную роль во многих естественных процессах, таких как формирование облаков, образование дождя и снега, а также конденсация водяного пара на поверхностях.
Изменения внутренней энергии при конденсации

Внутренняя энергия вещества определяется кинетической и потенциальной энергией его частиц. При конденсации происходит переход газообразного вещества в жидкое состояние. В этом процессе происходят значительные изменения внутренней энергии.
Когда газ переходит в жидкость, его частицы уплотняются и скапливаются вместе. Это приводит к увеличению потенциальной энергии системы, так как частицы вступают во взаимодействие друг с другом. При этом, кинетическая энергия частиц уменьшается, так как их скорости снижаются.
Увеличение потенциальной энергии и уменьшение кинетической энергии приводят к общему снижению внутренней энергии системы. Энергия, выделяющаяся при конденсации, передается окружающей среде, что обуславливает появление тепла.
Изменения внутренней энергии при конденсации могут быть использованы в различных процессах и технологиях. Например, при кондиционировании воздуха конденсацией удаляется избыточная влага из воздуха, а выделяющееся при этом тепло может быть использовано для обогрева помещений.
Таким образом, при конденсации происходит снижение внутренней энергии системы за счет увеличения потенциальной энергии и снижения кинетической энергии частиц. Выделение тепла при этом процессе позволяет использовать изменения внутренней энергии для различных практических целей.
Тепловые эффекты конденсации
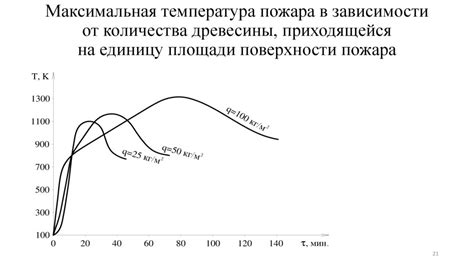
- Выделение тепла – один из основных тепловых эффектов конденсации. Во время конденсации газ теряет свою внутреннюю энергию, которая переходит в виде тепла окружающей среде. Это происходит потому, что молекулы газа, которые изначально двигались хаотично и обладали большой кинетической энергией, при сближении с поверхностью жидкости совершают микроскопические столкновения и передают свою кинетическую энергию молекулам жидкости. В результате этого процесса молекулы жидкости начинают двигаться быстрее и их температура повышается.
- Снижение температуры окружающей среды – еще один тепловой эффект конденсации, который наблюдается, когда конденсирующийся газ отбирает тепло из окружающей среды. Этот эффект может привести к охлаждению воздуха или других объектов, находящихся рядом с местом, где происходит конденсация.
Важно отметить, что тепловые эффекты конденсации могут быть полезными в различных технических и промышленных процессах. Например, воздухоочистители используют конденсацию для удаления влаги из воздуха, а холодильники и кондиционеры основаны на принципе охлаждения воздуха путем конденсации.
Переходная скорость и время конденсации
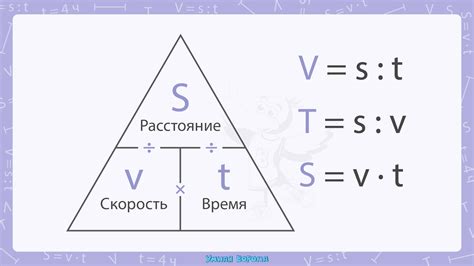
При конденсации пара в воздухе происходит переходная скорость, которая зависит от различных факторов, включая разницу в температуре между паром и окружающей средой, концентрацию пара и физические свойства воздуха.
Переходная скорость - это скорость, с которой пар превращается в жидкость при цельсийской температуре в известном объеме воздуха. Эта скорость может быть выражена как количество вещества, которое конденсируется за единицу времени и площадь поверхности, на которой происходит конденсация.
Время конденсации - это время, за которое все возможное количество пара конденсируется при конкретных условиях. Оно зависит от температуры, давления и влажности окружающей среды, а также от физических свойств пара, таких как скорость движения молекул и их средняя свободная длина.
Учитывая эти факторы, время конденсации может быть разным для различных веществ и условий окружающей среды. Для некоторых веществ конденсация может происходить очень быстро, в то время как для других может требоваться значительно больше времени.
Понимание переходной скорости и времени конденсации помогает в изучении процессов конденсации и позволяет предсказывать, какие условия могут быть оптимальными для конденсации определенных веществ.
Влияние давления и температуры на конденсацию
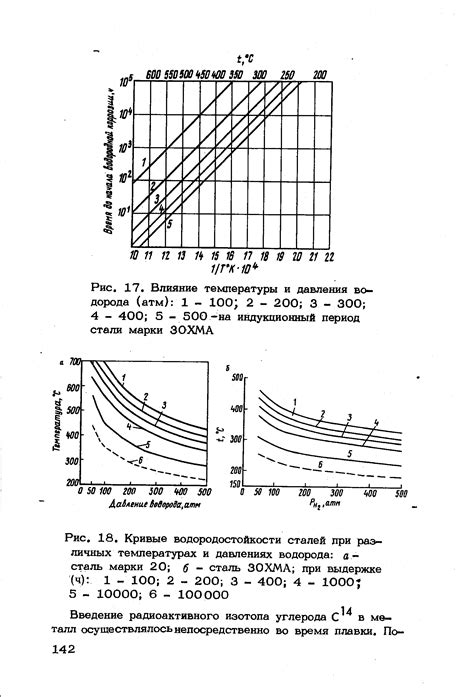
Увеличение давления способствует повышению температуры конденсации. При увеличении давления молекулы газа сближаются друг с другом, что обуславливает увеличение силы их притяжения и снижение количества кинетической энергии. В результате температура становится недостаточно высокой для поддержания газового состояния, и происходит конденсация.
Температура также оказывает влияние на конденсацию. При снижении температуры молекулы газа замедляют свои движения, кинетическая энергия уменьшается, и молекулы начинают сближаться. При определенной температуре газ переходит в жидкое состояние, происходит конденсация.
Повышение давления и снижение температуры являются взаимосвязанными факторами, которые в совокупности определяют условия конденсации вещества. Их взаимодействие оказывает важное влияние на изменение внутренней энергии системы и в результате приводит к конденсации газа в жидкость.
Практическое применение конденсации и контроль над внутренней энергией

Одно из основных практических применений конденсации – это выделение и очистка жидких компонентов из смесей газов. Например, в промышленности конденсацию применяют для получения чистого водяного пара из газовых смесей. Это позволяет использовать пар в дальнейшей технологической цепочке или для получения питьевой воды.
Кроме того, конденсацию можно использовать для разделения смесей различных жидкостей. При этом каждая компонента смеси имеет различную точку кипения, что позволяет разделить их в процессе конденсации. Такой метод активно применяется в химической и нефтехимической промышленности.
Одной из важных задач контроля над внутренней энергией является управление температурным режимом. Конденсация позволяет удалять из системы избыточное тепло, что особенно важно в процессе охлаждения и обеспечения эффективного функционирования различных устройств и механизмов.
В технике конденсация применяется, например, в системах кондиционирования и холодильных установках, где целью является охлаждение воздуха или хладагента. Благодаря процессу конденсации, избыточное тепло из системы удаляется, а жидкость переходит в газообразное состояние.
Контроль над внутренней энергией при конденсации также важен в физико-химических и медицинских исследованиях. Позволяет управлять скоростью протекания процессов и получать однородные образцы для более точного анализа их свойств.
Таким образом, практическое применение конденсации и контроль над внутренней энергией играют важную роль в различных отраслях, обеспечивая эффективность и надежность технологических процессов, очистку и выделение значимых компонентов и определение свойств веществ.