Состояние вещества является одним из основных понятий физики и химии. Различные вещества могут находиться в разных состояниях: газообразном, жидком или твердом. Определить состояние вещества может быть не так просто, но существуют определенные признаки и характеристики, которые помогают осуществить эту задачу.
Газообразные вещества характеризуются высокой подвижностью и низкой плотностью. Они могут заполнять любую доступную им объемную емкость. Кроме того, газы обычно расширяются при нагревании и сжимаются при охлаждении. Газы обычно не образуют определенной формы и не имеют определенного объема. Они также могут быть невидимыми или иметь цвет в зависимости от вещества.
Жидкости, в отличие от газов, обладают определенным объемом, который они сохраняют независимо от формы емкости. Жидкости также обладают плотностью и имеют определенную форму, которая может меняться в зависимости от объемной емкости. Одним из ключевых признаков жидкости является способность к течению и заниманию нижнего положения в емкости. Как и газы, жидкости расширяются при нагревании и сжимаются при охлаждении, но в незначительной степени.
Определение состояния вещества: газ, жидкость или твердое тело
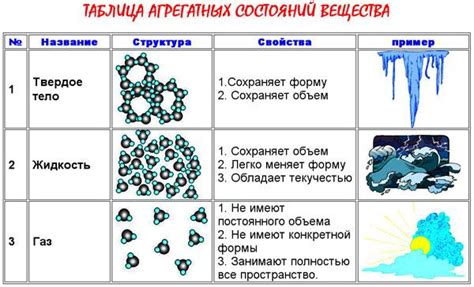
Определить состояние вещества можно, изучая его общие свойства. Одно из главных общих свойств - это форма.
Газы обладают формой, которая полностью зависит от контейнера, в котором они находятся. Их частицы располагаются хаотично и постоянно движутся. Примеры газов - кислород, водород, азот и прочие. Они обычно не имеют постоянного объема и формы, а могут изменять их в зависимости от воздействия внешних факторов.
Жидкость, в отличие от газа, обладает определенной формой и может заполнять не только верхнюю часть сосуда, но и его нижнюю часть. Внутри жидкости частицы движутся свободно, хаотично и более плотно упакованы по сравнению с газами. Примеры жидкостей - вода, ртуть, спирт, масло.
Твердые тела обладают фиксированной формой и объемом. Их частицы практически не двигаются и максимально плотно упакованы. Примеры твердых тел - металлы, полимеры, камни и другие.
Определение состояния вещества в повседневной жизни может быть осуществлено наблюдением за общими свойствами вещества, такими как форма и объем, а также отслеживанием его поведения при изменении температуры и давления.
Важно отметить:
- Определение состояния вещества имеет значение для понимания его физических свойств и реакций.
- Состояние вещества может изменяться при изменении температуры и давления.
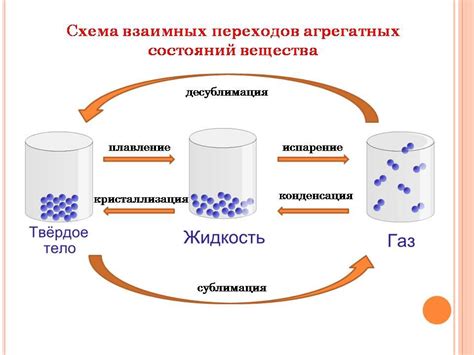
- Порядок изменения состояния вещества при изменении температуры: твердое тело - жидкость - газ.
- При переходе из одного состояния в другое могут происходить фазовые переходы, такие как плавление, кипение и т. д.
Определение состояния вещества является основой для понимания химических свойств и взаимодействий между веществами. Это помогает в различных областях науки и технологий, таких как химия, физика, медицина, инженерия и другие.
Физические свойства вещества, отвечающие за его состояние

Температура: Одним из важнейших параметров, определяющих состояние вещества, является его температура. При достаточно высокой температуре вещество может находиться в газообразном состоянии, при низкой температуре – в твердом состоянии, а при промежуточных значениях – в жидком состоянии.
Давление: Давление также играет важную роль в определении состояния вещества. При высоком давлении газы сжимаются, становятся жидкостью, а при низком давлении жидкости испаряются и переходят в газообразное состояние.
Межмолекулярные силы: Межмолекулярные силы взаимодействия молекул вещества также влияют на его состояние. В твердом теле межмолекулярные силы довольно сильные, что делает вещество прочным и неизменным в своей форме. В жидкостях межмолекулярные силы слабее, что позволяет им принимать форму сосуда, но сохранять свой объем. В газообразных веществах межмолекулярные силы очень слабы, и молекулы свободно движутся в пространстве.
Изменение плотности вещества при изменении его состояния
При изменении состояния вещество может переходить из твердого тела в жидкость и из жидкости в газ. В твердом теле молекулы вещества находятся очень близко друг к другу и плотность вещества обычно высокая. При переходе вещества в жидкое состояние молекулы начинают двигаться относительно друг друга, позволяя веществу принимать форму сосуда, в котором находится. Плотность вещества при этом снижается. В газообразном состоянии молекулы вещества находятся на большом расстоянии друг от друга и плотность вещества минимальна.
Например, плотность воды в твердом состоянии (лед) составляет около 0,9167 г/см³, в жидком состоянии - около 1 г/см³, а в газообразном состоянии (пар) - около 0,0006 г/см³.
Изменение плотности вещества при переходе из одного состояния в другое имеет важное практическое значение, так как позволяет использовать различные вещества в разных состояниях для разных целей. Например, вода в твердом состоянии (лед) используется для охлаждения, в жидком состоянии - для питья и приготовления пищи, а в газообразном состоянии (пар) - для процессов обогрева и привода. Понимание изменения плотности вещества при изменении его состояния важно для многих областей научных и технических исследований.
Точки плавления и кипения вещества как показатели состояния

Точка плавления – это температура, при которой вещество переходит из твердого состояния в жидкое состояние при постоянном давлении. При достижении точки плавления между атомами или молекулами вещества нарушается упорядоченность, а связи становятся подвижными. Точка плавления является характеристикой каждого вещества и может быть выражена в градусах Цельсия.
Точка кипения – это температура, при которой вещество переходит из жидкого состояния в газообразное состояние при постоянном давлении. При достижении точки кипения между атомами или молекулами вещества происходит разрыв связей, что приводит к образованию газовых молекул. Точка кипения также является индивидуальной характеристикой каждого вещества и измеряется в градусах Цельсия.
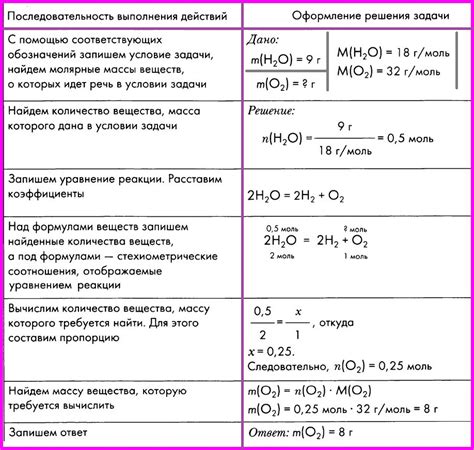
Таблица ниже приводит примеры точек плавления и кипения для некоторых веществ:
| Вещество | Точка плавления (°C) | Точка кипения (°C) |
|---|---|---|
| Вода | 0 | 100 |
| Железо | 1538 | 2862 |
| Кислород | -218.79 | -183 |
Из таблицы видно, что вода находится в жидком состоянии при комнатной температуре, так как точка плавления выше 0°C, а точка кипения ниже 100°C. Железо является твердым телом, так как обе точки выше комнатной температуры. Кислород находится в газообразном состоянии при комнатной температуре, так как точка кипения ниже -183°C.
Молекулярная структура и форма частиц вещества
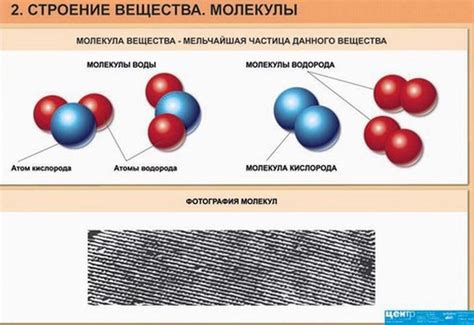
В газообразных веществах молекулы находятся на большом расстоянии друг от друга и движутся хаотично в разных направлениях. Они обладают высокой подвижностью и свободно заполняют имеющееся пространство. Форма и объем газообразного вещества зависят от его контейнера.
В жидкостях молекулы ближе друг к другу и они образуют тесные взаимосвязи. Они несвободно двигаются, совершая взаимопроникновение и перемешивание. Жидкости имеют определенный объем, но их форма может изменяться.
Твердые тела обладают наиболее плотной и упорядоченной структурой. Молекулы или атомы твердого вещества тесно связаны друг с другом и не совершают значительного движения. Твердые тела имеют определенную форму и объем, которые сохраняются независимо от контейнера.
Таким образом, молекулярная структура и форма частиц вещества определяют его состояние и свойства. Понимание этих особенностей помогает нам классифицировать и понимать различные вещества в нашей ежедневной жизни.
Диффузия вещества в зависимости от его состояния
В газах диффузия происходит наиболее быстро. Это связано с тем, что молекулы газов расположены свободно и сильно двигаются в случайных направлениях. Молекулы газа сталкиваются друг с другом и меняют свою скорость и направление движения, что позволяет им быстро перемещаться через пространство. Примером диффузии в газах может служить запах, который распространяется и заполняет всю доступную область равномерно.
В жидкостях диффузия происходит уже медленнее. Жидкости имеют более плотную структуру молекул, что затрудняет их перемещение. Молекулы жидкости все же могут перемещаться, но процесс диффузии замедлен. Примером может служить распространение красителя в воде - изначально капля красителя располагается в одной точке, но со временем он распределяется равномерно по всему объему воды.
Твердые тела имеют наиболее медленную диффузию. Причина этого заключается в том, что молекулы твердых тел плотно упакованы и мало двигаются. Диффузия в твердых телах может происходить только при наличии свободных дырок в кристаллической решетке. Примером диффузии в твердых телах может служить распространение примесей в металле или диффузия тепла через полностью нагретый стержень.
Таким образом, скорость диффузии вещества зависит от его состояния. Газы диффундируют быстрее, жидкости - медленнее, а твердые тела имеют самую медленную диффузию.
Скорость распространения звука в веществе и его связь с состоянием
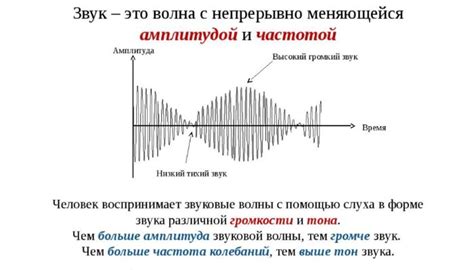
В газах молекулы находятся на больших расстояниях друг от друга и движутся хаотически. При передаче звука в газе между молекулами передается колебательное движение, и скорость звука в газе достигает высоких значений. Например, воздуха скорость звука при комнатной температуре составляет около 343 метра в секунду.
В жидкостях молекулы находятся ближе друг к другу, но все равно имеют возможность двигаться. Это влияет на скорость распространения звука в жидкости, которая обычно меньше, чем в газе. Например, в воде скорость звука составляет около 1482 метра в секунду.
В твердых телах молекулы или атомы плотно упакованы и не имеют возможности свободно перемещаться. Они могут передавать звук только через колебания вещества. В результате скорость звука в твердых телах обычно наибольшая. Например, в стали скорость звука составляет около 5820 метров в секунду.
Таким образом, скорость распространения звука в веществе связана с его состоянием, где газы имеют наибольшую скорость, затем следуют жидкости, а потом твердые тела.
Воздействие внешних факторов на состояние вещества

Состояние вещества может изменяться под воздействием различных внешних факторов, таких как температура и давление. Эти факторы играют ключевую роль в определении, будет ли вещество находиться в газообразной, жидкой или твердой форме.
При повышении температуры частицы вещества приобретают больше энергии и начинают двигаться быстрее. Как только энергия частиц становится достаточной для преодоления сил притяжения, вещество переходит из твердого состояния в жидкое (плавление) или из жидкого в газообразное (кипение).
Давление также влияет на состояние вещества. Под действием высокого давления между частицами вещества возникают сильные силы притяжения, что делает их более уплотненными и в результате вещество становится твердым. Напротив, при низком давлении силы притяжения между частицами снижаются, что позволяет им свободно двигаться, и вещество переходит в газообразное состояние.
Некоторые вещества могут переходить между состояниями при изменении как температуры, так и давления. Например, вода при нормальных условиях является жидкостью, но при пониженных температурах она может замерзать и становиться твердой, а при повышенном давлении - кипеть и переходить в пар.
Понимание влияния внешних факторов на состояние вещества является важным для многих областей науки и технологий, таких как химия, физика и инженерия. Изучение этих зависимостей помогает разрабатывать новые материалы и оптимизировать процессы в различных индустриях.
Реакции веществ при изменении состояния
При изменении состояния вещества, например, при нагревании или охлаждении, происходят различные химические и физические реакции. Они могут приводить к образованию новых соединений или изменению свойств существующих.
При переходе из одного состояния вещества в другое происходят различные реакции. Например, при нагревании твердого вещества оно может превратиться в жидкость или газ. Этот процесс называется плавлением или испарением. При плавлении или испарении происходят физические изменения, а не химические реакции.
Однако при нагревании или охлаждении вещества могут происходить и химические реакции. Например, при нагревании угля в атмосфере кислорода происходит его сгорание, при котором образуется углекислый газ. Это химическая реакция, при которой происходят изменения в составе вещества.
Также изменение состояния вещества может приводить к образованию новых соединений. Например, при охлаждении пара воды она может конденсироваться и превратиться в жидкость. Этот процесс сопровождается образованием капель воды и является физическим изменением. Однако, при дальнейшем охлаждении или при наличии других веществ, могут происходить химические реакции, приводящие к образованию новых соединений.
Изменение энергетического состояния вещества при переходе между состояниями
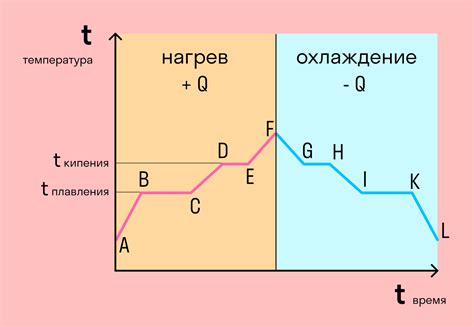
Переход вещества из одного состояния в другое сопровождается изменением его энергетического состояния. При этом вещество поглощает или отдает определенное количество энергии.
Переход от твердого состояния к жидкому состоянию называется плавлением. В этом случае, чтобы преодолеть силы притяжения между атомами или молекулами, необходимо добавить энергию. При плавлении твердого вещества энергия извне вызывает возрастание теплового движения молекул, что приводит к увеличению промежутков между ними и образованию неупорядоченной структуры - жидкости.
Для перехода от жидкого состояния к газообразному состоянию требуется дополнительное количество энергии. В этом случае молекулы образуют пары, преодолевая силы притяжения между ними. Такой процесс называется испарением. Чем выше энергия молекул, тем активнее происходит их испарение.
Обратным процессом к испарению является конденсация - переход из газообразного состояния к жидкому. При конденсации происходит освобождение энергии, которая передается окружающей среде в виде тепла.
Для перехода от жидкого состояния к твердому состоянию (замерзание) требуется еще больше энергии, так как молекулы должны упорядочиться и образовать кристаллическую структуру.
| Состояние вещества | Энергия |
|---|---|
| Твердое | Низкая |
| Жидкое | Средняя |
| Газообразное | Высокая |
Таким образом, при переходе между состояниями вещества происходит изменение его энергетического состояния. Это важный аспект, который позволяет понять, какие процессы происходят внутри вещества при изменении условий окружающей среды.
Примеры веществ в различных состояниях и их применение
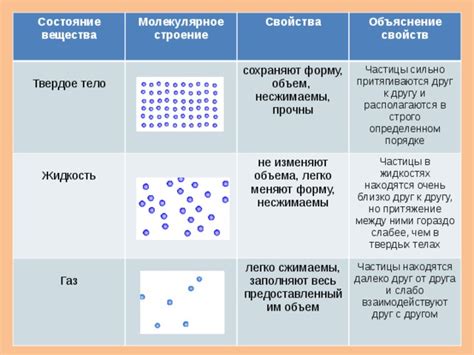
В природе существует множество веществ, которые могут находиться в различных состояниях: газообразном, жидком и твердом. Вот некоторые примеры и их применение:
Газообразные вещества:
Кислород (O2): используется в медицине для поддержания дыхания, а также в производстве стали и горючих смесей.
Водород (H2): используется в производстве аммиака, воды и водородной энергетике.
Углекислый газ (CO2): используется в газоходообменной аппаратуре, производстве газожидкостных материалов и газовых наполнителей.
Жидкие вещества:
Вода (H2O): используется во многих сферах, включая пищевую промышленность, химическую промышленность, а также в быту и сельском хозяйстве.
Нефть: используется для производства бензина, дизельного топлива, пластиков, асфальта и других нефтепродуктов.
Этиловый спирт (C2H5OH): используется в медицине, химической промышленности, косметике и в производстве алкогольных напитков.
Твердые вещества:
Алмаз: используется в ювелирном и индустриальном производстве, а также в научных исследованиях.
Железо: используется в строительстве, машиностроении, производстве стали и других металлических изделий.
Сахар (сахароза): используется в пищевой промышленности, в производстве кондитерских изделий и напитков.
Это всего лишь несколько примеров веществ, которые могут находиться в различных состояниях и иметь различное применение. Их химические и физические свойства определяют, каким образом они могут быть использованы в различных отраслях науки, промышленности и повседневной жизни.