Расчет массы вещества по массовой доле является важной задачей в химии и физике. Массовая доля показывает, какую долю массы занимает искомое вещество в смеси. В данной статье мы рассмотрим, как просто и быстро определить массу вещества при известной массовой доле.
Для проведения расчета необходимо знать массу смеси и массовую долю искомого вещества. Массовая доля представляет собой отношение массы искомого вещества к массе смеси и выражается в процентах или доли единицы.
Для начала необходимо определить массу искомого вещества в смеси. Для этого умножаем массу смеси на массовую долю, представленную в виде десятичной дроби. Полученное число будет равно массе искомого вещества в граммах или килограммах.
Таким образом, расчет массы вещества по массовой доле является простым и эффективным методом определения количества искомого вещества в смеси. Умение проводить такие расчеты является необходимым навыком для химиков и физиков, и может быть полезным в различных областях науки и промышленности.
Что такое массовая доля

Массовая доля выражается в процентах, иначе говоря, величиной от 0 до 100. Например, если массовая доля определенного элемента в смеси равна 30%, это означает, что 30 граммов этого элемента содержатся в каждых 100 граммах смеси.
Массовая доля является неотъемлемой частью химических расчетов и анализов. Она позволяет определить, насколько концентрировано или разбавлено вещество в растворе или смеси. Кроме того, массовую долю можно использовать для расчета количества вещества, которое нужно добавить или извлечь из смеси.
Для вычисления массовой доли необходимо знать массу вещества и массу всей смеси или соединения. Формула для расчета массовой доли выглядит следующим образом:
Массовая доля (в %) = (Масса вещества / Масса смеси или соединения) * 100
Например, если масса вещества равна 20 граммам, а масса смеси – 100 граммам, то массовая доля будет равна (20 / 100) * 100 = 20%.
Массовая доля играет важную роль в различных областях, включая химию, фармацевтику, пищевую промышленность и др. Знание массовой доли помогает контролировать процессы смешивания веществ, анализировать качество продукции и разрабатывать новые формулы и составы.
Способы нахождения массы вещества по массовой доле

1. По формуле массовой доли:
Масса вещества = (Массовая доля × Масса смеси) / 100%
Данная формула позволяет найти массу исследуемого вещества, зная его массовую долю и массу смеси или раствора.
2. По молярной массе:
Масса вещества = (Массовая доля × Количество вещества × Молярная масса) / 100%
Если известно количество вещества в молях и его массовая доля, можно найти массу с использованием молярной массы вещества.
3. С использованием метода разведения:
Данный метод используется при наличии растворов различной концентрации. Путем разведения раствора с известной массовой долей до требуемой концентрации и измерения массы полученного раствора можно найти массу исследуемого вещества.
В зависимости от поставленной задачи и доступной информации можно выбрать наиболее удобный и точный способ нахождения массы вещества по массовой доле. При этом следует учитывать все имеющиеся данные и использовать соответствующие формулы и методы решения задачи.
Способ 1: Масса вещества и массовая доля других компонентов

Для того чтобы найти массу вещества по известной массовой доле других компонентов, необходимо выполнить несколько простых шагов. Для начала, следует определить общую массу смеси, в которой находится вещество и другие компоненты. Затем, необходимо вычислить массовую долю каждого компонента в смеси, используя специальные формулы или таблицы.
Массовая доля вычисляется как отношение массы конкретного компонента к общей массе смеси. Например, если общая масса смеси равна 100 граммам, а масса компонента А составляет 20 грамм, то его массовая доля будет равна 20% (20 грамм / 100 грамм * 100% = 20%).
Теперь, имея массовую долю каждого компонента в смеси, можно найти массу исследуемого вещества. Для этого необходимо умножить массовую долю исследуемого вещества на общую массу смеси. Например, если массовая доля исследуемого вещества составляет 30%, а общая масса смеси равна 200 граммам, то масса исследуемого вещества будет равна 60 граммам (30% * 200 грамм = 60 грамм).
Таким образом, используя данный способ, можно найти массу вещества по массовой доле других компонентов в смеси. Важно помнить, что массовая доля должна быть задана в процентах, а общая масса смеси должна быть измерена в граммах или килограммах.
Способ 2: Массовая доля и объем вещества

Для расчета массы вещества по массовой доле и объему вещества необходимо использовать следующую формулу:
Масса вещества = объем вещества × массовая доля вещества ÷ 100
Применение данной формулы позволяет определить массу вещества по результатам измерений массовой доли и объема вещества. Например, если измерения показали, что массовая доля вещества составляет 40%, а объем вещества в смеси составляет 100 мл, то масса вещества будет равна:
Масса вещества = 100 мл × 40% ÷ 100 = 40 мл
Таким образом, масса вещества в данном случае будет равна 40 г.
Способ 3: Массовая доля и плотность вещества

Массовая доля (молярная доля) - это отношение массы исследуемого вещества к общей массе смеси. Она выражается в процентах или десятичных долях.
Плотность вещества - это отношение массы вещества к его объему. Она характеризует степень компактности исследуемого вещества и выражается в г/см³ или кг/м³.
Чтобы найти массу вещества, используя массовую долю и плотность вещества, нужно умножить массовую долю на массу или объем смеси и затем умножить полученное значение на плотность вещества. Формула для расчета выглядит следующим образом:
Масса вещества = Массовая доля × Масса (Объем) смеси × Плотность вещества
Примером может служить ситуация, когда известно, что массовая доля соли в растворе составляет 10%, а плотность раствора равна 1 г/см³. Если известен объем раствора, то можно использовать следующую формулу для определения массы соли:
Масса соли = 0,1 × Объем раствора × 1 г/см³
Таким образом, зная массовую долю и плотность вещества, можно рассчитать массу вещества в смеси.
Способ 4: Массовая доля и количество молей вещества

Массовая доля выражается в процентах и показывает, какая часть массы образца приходится на искомый элемент. Количество молей вещества показывает, сколько частиц данного вещества содержится в образце.
Чтобы найти массу вещества по массовой доле и количеству молей вещества, нужно использовать следующую формулу:
Масса вещества = массовая доля × масса образца ÷ количество молей вещества
Применение этой формулы поможет легко и точно определить массу искомого вещества в образце.
Пример:
Образец содержит 50 г вещества, массовая доля искомого элемента составляет 10%, что соответствует 0.1 моль вещества. С помощью формулы найдем массу искомого элемента в данном образце:
Масса вещества = 0.10 × 50 г ÷ 0.1 моль = 50 г
Таким образом, масса искомого элемента в данном образце составляет 50 г.
Способ 5: Массовая доля и процентное содержание вещества
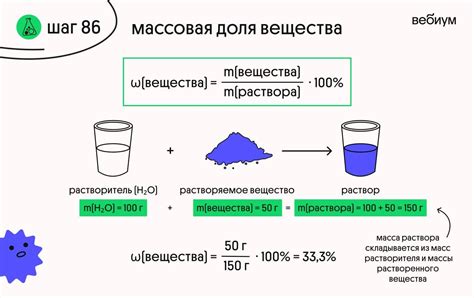
Массовая доля и процентное содержание вещества используются для определения количества определенного вещества в смеси или растворе. Этот метод подразумевает нахождение отношения массы вещества к массе всей смеси и выражение его в процентах.
Для расчета массовой доли вещества в смеси или растворе, следует использовать следующую формулу:
Массовая доля (%) = (Масса вещества / Масса смеси или раствора) * 100
Для расчета процентного содержания вещества, достаточно умножить массовую долю на 100. Обозначается формулой:
Процентное содержание (%) = Массовая доля * 100
| Величина | Обозначение |
|---|---|
| Масса вещества | Масса вещества в смеси или растворе |
| Масса смеси или раствора | Общая масса смеси или раствора |
| Массовая доля | Отношение массы вещества к массе смеси или раствора |
| Процентное содержание | Выражение массовой доли в процентах |
Этот способ позволяет точно определить массу вещества в смеси или растворе, что является важным этапом в химических и аналитических исследованиях. Он широко применяется в медицине, фармакологии, пищевой промышленности и других отраслях науки и техники.
Способ 6: Массовая доля и количество атомов вещества

Чтобы найти массу вещества по массовой доле и известной общей массе вещества, необходимо:
- Рассчитать количество моль вещества с использованием молярной массы вещества.
- Пересчитать количество моль компонента, зная массовую долю компонента.
- Найти массу компонента, используя массу вещества и количество моль компонента.
Применяя этот метод, можно также найти количество атомов компонента, используя его массовую долю и количество атомов в молекуле вещества. Для этого необходимо умножить массовую долю компонента на количество молекул вещества и умножить результат на количество атомов данного компонента в молекуле вещества.
Подобным образом можно рассчитать и количество молекул компонента, зная его массовую долю и количество молекул в веществе.
| Величина | Формула |
|---|---|
| Масса вещества | Масса = молярная масса × количество моль вещества |
| Количество атомов компонента | Количество атомов = массовая доля × количество молекул вещества × количество атомов в молекуле компонента |
| Количество молекул компонента | Количество молекул = массовая доля × количество молекул вещества |
Способ 7: Массовая доля и молекулярная масса вещества
При работе с химическими реакциями часто возникает необходимость определить массу вещества по его массовой доле. Для этого используется формула:
| Массовая доля | Масса вещества | Молекулярная масса |
|---|---|---|
| х | м | М |
где х - массовая доля вещества, м - масса вещества, М - молекулярная масса вещества.
Чтобы найти массу вещества, нужно умножить массовую долю на молекулярную массу:
м = х * М
Этот способ особенно полезен при проведении химических расчетов, когда известна массовая доля определенного компонента в смеси или соединении.
Обратите внимание, что массовая доля всегда выражается в процентах или долях (дробях), а масса вещества должна быть выражена в одних и тех же единицах, что и молекулярная масса (например, граммах или килограммах).
Используя способ 7, вы сможете легко определить массу вещества по его массовой доле, применяя данную формулу и используя известные значения массовой доли и молекулярной массы. Таким образом, вы сможете более точно контролировать и расчитывать химические реакции и процессы в своих экспериментах.