В химии, одной из основных наук, изучающих состав и свойства веществ, концентрация реагирующих веществ является важной характеристикой, определяющей эффективность химических реакций. Концентрация позволяет определить количество вещества, содержащегося в определенном объеме или массе раствора или смеси.
Концентрация реагирующих веществ может быть выражена различными способами, такими как молярность, мольная доля, процентное содержание и другие. Но в целом концентрация показывает, насколько плотно вещество упаковано в растворе или смеси. Чем выше концентрация, тем больше активных частиц вещества присутствует на единицу объема или массы, что способствует более интенсивным химическим реакциям.
Концентрация реагирующих веществ играет важную роль в различных областях химии. В органической химии, например, концентрация реагентов может определять скорость реакции и получение желаемого продукта. В аналитической химии концентрация используется для определения содержания веществ в образцах методами количественного анализа.
Поэтому точное определение и контроль концентрации реагирующих веществ - важные задачи для химиков и научных исследователей. Он позволяет предсказать результаты реакции, проводить эксперименты в оптимальных условиях и добиваться желаемых химических превращений. Но также важно помнить, что концентрация вещества может влиять на его токсичность и вредность для окружающей среды, поэтому контроль ее уровня необходим также для обеспечения безопасности и экологической устойчивости процессов химической промышленности.
Определение концентрации реагирующих веществ

Часто концентрация выражается в виде молярности – количества вещества, выраженного в молях, на единицу объема раствора или системы (моль/л или М). Другими популярными единицами измерения концентрации являются процентное содержание, доли или доля равновесия.
Для определения концентрации реагирующих веществ используются различные методы и вычислительные формулы, которые учитывают знание начальных и конечных состояний системы. Например, при известном объеме раствора, количество вещества с использованием уравнения Нернста может быть выражено через изменение потенциала электрода.
Концентрация реагирующих веществ имеет важное значение для понимания и предсказания химических реакций. Она позволяет рассчитать количество продуктов, получаемых в результате реакции, а также оценить скорость реакции и эффективность процесса.
Понятие концентрации в химии

Одним из наиболее распространенных методов выражения концентрации является молярность. Молярность определяет количество вещества, выраженное в молях, содержащееся в одном литре раствора. Данный метод позволяет легко проводить расчеты и сравнивать концентрации различных реагентов.
Еще одним способом выражения концентрации является массовая концентрация. Она указывает на количество массы вещества, растворенного в определенном объеме растворителя. Массовая концентрация может быть выражена в процентах (%), долях (дробях) или граммах на литр (г/л).
Для более точного определения концентрации вещества в часто малых концентрациях используются такие понятия, как моляльность и нормальность. Моляльность выражает количество вещества, находящегося в одном килограмме растворителя. Нормальность указывает на количество активных частиц реагента, участвующих в реакции, в одном литре раствора.
Важно отметить, что концентрация вещества влияет на скорость химической реакции. Чем выше концентрация реагентов, тем быстрее протекает реакция. Кроме того, правильное определение концентрации позволяет более точно контролировать процесс синтеза и получение продукта.
Таким образом, понятие концентрации в химии является важным для понимания и изучения химических реакций. Оно позволяет определить количество реагирующих веществ в системе и контролировать ход процесса.
Методы измерения концентрации

Один из наиболее распространенных методов измерения концентрации - титрование. Этот метод основан на точном измерении объема раствора добавленного вещества, необходимого для полного определения концентрации реагирующего вещества. Титрование позволяет определить концентрацию с высокой точностью, однако требует использования точных объеметрических приборов и специальных индикаторов, которые меняют окраску при достижении эквивалентной точки реакции.
Еще одним методом измерения концентрации является спектрофотометрия. С помощью спектрофотометра измеряется оптическая плотность раствора, которая зависит от концентрации вещества в растворе. Путем построения калибровочной кривой можно определить концентрацию неизвестного вещества в растворе. При этом важно выбрать подходящую длину волны, на которой абсорбция вещества максимальна.
Еще одним способом измерения концентрации является весовой метод. Он заключается в определении массы творящего вещества и его объема или массы растворимого вещества в определенном объеме раствора. При этом следует учитывать плотность вещества и другие физические свойства, которые могут влиять на точность результатов.
Также существуют более сложные методы измерения концентрации, такие как газовая хроматография, жидкостная хроматография, масс-спектрометрия и др. Эти методы позволяют определить концентрацию вещества с высокой чувствительностью и выбороскостью, однако требуют специального оборудования и экспертизы.
Важно отметить, что выбор метода измерения концентрации зависит от свойств и требований реагирующих веществ, доступности и возможностей лаборатории, а также требуемой точности и скорости измерений.
Значение концентрации для химических реакций

Концентрация реагирующих веществ имеет важное значение в химических реакциях. Она определяет количество реагентов, присутствующих в определенном объеме реакционной среды. Концентрация влияет на скорость реакции, выбор продуктов реакции и общий ход химического процесса.
Концентрация реагентов может быть выражена в различных единицах измерения, таких как молярность, мольная доля и процентная концентрация. Молярность определяет количество вещества в растворе на единицу объема, выраженное в молях на литр. Мольная доля показывает отношение числа молей данного реагента к общему числу молей всех реагентов. Процентная концентрация указывает на долю реагента в растворе в процентах. Эти единицы измерения позволяют химикам точно определять количество реагентов, задействованных в реакции.
Значение концентрации также влияет на равновесие химической реакции. По принципу Ле Шателье, изменение концентрации одного из реагентов или продуктов приводит к восстановлению равновесия химической системы. Повышение концентрации реагента может ускорить химическую реакцию, тогда как снижение концентрации может замедлить ее или даже привести к обратной реакции.
Концентрация реагентов также может быть использована для расчета выхода продуктов реакции. Зная начальные концентрации реагентов и коэффициенты их участия в реакции, химики могут определить, сколько продуктов будет образовано и какое количество реагентов останется неизрасходованным.
В целом, значение концентрации реагирующих веществ в химии нельзя недооценивать. Она является ключевым фактором, влияющим на ход и результаты химических реакций. Правильное определение и контроль концентрации позволяет улучшить эффективность и предсказуемость химических процессов.
Влияние концентрации на скорость реакции
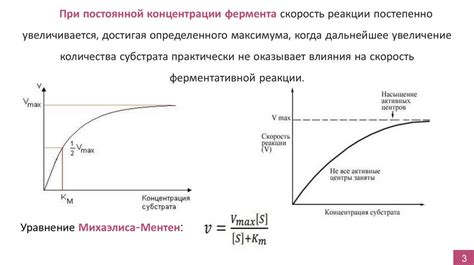
Увеличение концентрации реагентов в химической реакции приводит к повышению вероятности их столкновения и, следовательно, увеличению скорости реакции. Это объясняется тем, что большее количество реагирующих частиц создает более благоприятные условия для взаимодействия между ними.
Согласно теории столкновений, частицы должны иметь достаточную энергию, чтобы преодолеть энергетический барьер и вступить в химическую связь. Повышение концентрации реагентов увеличивает число столкновений, тем самым увеличивая вероятность столкновений с достаточной энергией для успешной реакции.
Следует отметить, что изменение концентрации не влияет на энергию активации реакции, то есть на минимальную энергию, необходимую для начала реакции. Однако, повышение концентрации может значительно ускорить реакцию, так как частицы будут сталкиваться чаще и с большей энергией.
Важно отметить, что влияние концентрации на скорость реакции зависит от порядка реакции. В случае прямой реакции, увеличение концентрации реагентов приведет к увеличению скорости реакции, в то время как в случае обратной реакции, увеличение концентрации продуктов будет приводить к увеличению скорости реакции в обратном направлении.
Резюмируя, концентрация реагирующих веществ играет важную роль в определении скорости химической реакции. Увеличение концентрации приводит к увеличению числа столкновений и, следовательно, к увеличению скорости реакции. Однако, влияние концентрации на скорость реакции может различаться в зависимости от типа реакции.