Каталитические реакции - это химические процессы, при которых специальные вещества, называемые катализаторами, ускоряют химическую реакцию без изменения самих катализаторов. Термин "каталитическая реакция" происходит от греческого слова "κατάλυση", что означает "рассасывание" или "разрушение". Каталитические реакции играют важную роль в промышленности, жизни и окружающей среде, благодаря своей способности повышать эффективность реакций и снижать их энергетическую стоимость.
Катализаторы - это вещества, которые ускоряют химическую реакцию без участия в ней. Они понижают энергию активации реакции, что позволяет молекулам переходить из одного состояния в другое с меньшим затратами энергии. Катализаторы остаются практически без изменений в конце реакции и могут применяться многократно. Это делает их экономически выгодными и эффективными.
Каталитические реакции нашли широкое применение в различных отраслях промышленности. Они используются в производстве пластмасс, удобрений, лекарственных препаратов, красителей, пищевых добавок и технологий очистки воды и воздуха. Катализаторы также играют роль в жизни организмов, ускоряя химические реакции, необходимые для поддержания жизнедеятельности организма.
Что такое каталитические реакции?

В ходе каталитической реакции катализатор не исчезает и может использоваться неоднократно, обеспечивая повышение скорости реакции. Процесс каталитической реакции может быть представлен схемой:
Реакционные вещества + катализатор → Продукты реакции + катализатор
Основным свойством каталитических реакций является изменение энергетического барьера, который должны преодолеть реагенты для перехода в продукты реакции. Катализаторы способны снижать этот барьер, что приводит к ускорению реакции.
Каталитические реакции имеют большое значение в промышленности и научных исследованиях. Они позволяют получать продукты реакции более эффективно, снижая температуру и давление, а также сокращая время проведения процессов.
Определение и принцип действия
Основной принцип действия каталитических реакций состоит в том, что катализатор предоставляет альтернативный механизм реакции с меньшей энергией активации. Это позволяет ускорить скорость реакции и снизить температуру и давление, необходимые для ее проведения. Таким образом, катализаторы значительно экономят энергию и снижают затраты производства.
Кроме того, катализаторы могут повысить селективность реакции, направляя ее по определенному пути и образуя желаемые продукты. Они также могут увеличить стабильность реакционной системы и предотвратить побочные реакции.
Важно отметить, что катализаторы сами не расходуются в реакции и могут использоваться многократно. Они участвуют в начальной стадии реакции (образуют комплексы с исходными веществами), затем реакция протекает с их участием, и в конце они вновь высвобождаются в неизмененном виде.
Важность каталитических реакций
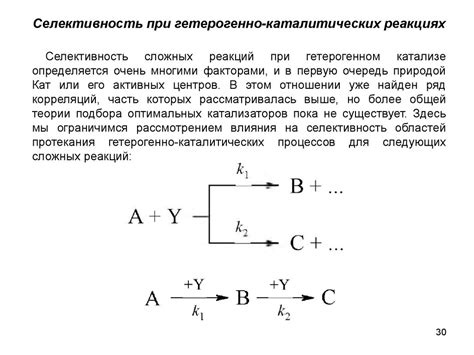
Каталитические реакции играют важную роль в химии и промышленности. Они позволяют увеличить скорость химических превращений при снижении температуры и энергии активации. Это особенно важно для таких процессов, которые происходят при низких температурах и требуют больших энергетических затрат.
Каталитические реакции позволяют совершать такие процессы, как окисление, присоединение и разрыв связей, образование циклических соединений и многие другие. Благодаря каталитическим реакциям возможна синтез и получение различных соединений, включая органические и неорганические вещества, а также лекарственные препараты и полимеры.
Каталитические реакции также играют важную роль в экологии и охране окружающей среды. Они позволяют уменьшить выбросы вредных веществ и улучшить качество воздуха, воды и почвы. Кроме того, каталитические реакции облегчают переработку отходов и повышают энергоэффективность производственных процессов.
Важность каталитических реакций подчеркивается их применением в различных отраслях промышленности, включая нефтепереработку, производство химических веществ, пищевую промышленность, электронику и многие другие. Каталитические реакции позволяют сократить время производства и снизить затраты ресурсов, что способствует экономическому развитию и повышению конкурентоспособности предприятий.
Каталитические реакции являются существенным элементом современной химии и имеют огромное значение для экономики, экологии и общества в целом.