Определение массы горящего вещества является одной из важных задач в химической и пиротехнической промышленности, позволяющей обеспечить безопасность процесса и получить желаемый результат. Расчет массы горящего вещества необходим для подбора оптимальных условий сгорания, а также для оценки эффективности химических реакций и прогнозирования их исхода.
Существует несколько методов определения массы горящего вещества, но одной из самых распространенных является использование химической формулы. Для этого необходимо знать химический состав горящего вещества и его молярную массу. Формула расчета массы горящего вещества выглядит следующим образом:
Масса = Молярная масса x Количество вещества
Количество вещества можно определить по таким показателям, как масса или объем вещества, а также его концентрация. Для определения молярной массы необходимо знать атомные массы элементов, входящих в состав горящего вещества, и их соотношение. По результатам расчета можно определить точную массу горящего вещества и использовать эту информацию для планирования и проведения химических экспериментов и процессов.
Постоянное обновление данных о химических соединениях и развитие новых методов расчета позволяет уточнить и улучшить точность определения массы горящего вещества. Это имеет большое значение для различных отраслей промышленности и науки, где безопасность и качество результатов являются приоритетами.
Что такое масса горящего вещества
Масса горящего вещества может быть определена различными методами, в зависимости от конкретной ситуации и химического соединения. Одним из способов определения массы горящего вещества является использование химических формул и реакций, которые представляют собой математическое выражение химического взаимодействия и массового баланса.
Для определения массы горящего вещества можно также использовать экспериментальные методы, например, с помощью взвешивания сосуда с веществом до и после сгорания. Такой подход является достаточно точным, но требует наличия достоверных данных о плотности и составе вещества.
Масса горящего вещества играет важную роль при проектировании систем пожаротушения, разработке мер по пожарной безопасности и оценке рисков возгорания. Знание точной массы горящего вещества позволяет правильно рассчитать необходимое количество огнетушащего вещества или воды для тушения пожара, а также эффективность применяемых средств.
Понимание массы горящего вещества является важным аспектом в химии и технике безопасности. Знание этого параметра позволяет обеспечить безопасные условия работы с горючими материалами и эффективно предупреждать и ликвидировать пожары.
Значение определения массы горящего вещества

Значение определения массы горящего вещества особенно важно в химических и физических экспериментах. В химических реакциях, где задействованы горящие вещества, знание и контроль массы горючего вещества позволяет установить баланс реакции и произвести расчеты по количеству продуктов.
Другим примером, где определение массы горящего вещества играет важную роль, может быть изучение термохимических процессов. При проведении термохимических экспериментов мы можем определить количество выделяющейся или поглощающейся энергии в зависимости от массы горючего вещества.
Определение массы горящего вещества также может быть полезным при исследовании воздействия различных факторов на горючие вещества. Зная массу горюшего вещества в определенных условиях, мы можем оценить степень его воспламеняемости и определить безопасные пределы эксплуатации.
Итак, определение массы горящего вещества является неотъемлемой частью проведения экспериментов и исследований в различных областях науки. Оно позволяет получить надежные данные, повышает точность результатов, а также способствует лучшему пониманию химических и физических процессов, связанных с горением веществ.
Методы определения массы горящего вещества

1. Планиметрический метод.
Этот метод основан на использовании графических методов измерения. С помощью специальных инструментов, таких как планиметр или карандашный планшет, измеряют площади горения горящего вещества на поверхности.
2. Водородный метод.
В этом методе масса горящего вещества определяется на основе реакции горения вещества с водородом. В ходе реакции выделяется водяной пар, который затем стирается проницаемым материалом. Изменение массы после процедуры стирания указывает на массу горящего вещества.
3. Взвешивание.
Самый простой способ определить массу горящего вещества - это взвесить его. Для этого используются весы, которые могут быть электронными или механическими. При этом необходимо учесть массу подложки, на которой находится горящее вещество.
4. Количественный анализ продуктов горения.
Для определения массы горящего вещества можно также использовать количественный анализ продуктов горения. После горения вещества продукты собираются и анализируются с помощью специального оборудования. На основе полученных данных рассчитывается масса горящего вещества.
Выбор метода определения массы горящего вещества зависит от его физико-химических свойств и целей эксперимента. Каждый метод имеет свои достоинства и ограничения, поэтому важно выбрать наиболее подходящий метод для конкретной задачи.
Метод взвешивания

Для проведения взвешивания горящего вещества необходимо:
- Подготовить аналитические весы и взвешивательные гири.
- Установить пустой контейнер на платформу весов.
- Откалибровать весы, приравняв ноль к показанию без контейнера.
- Осторожно поместить образец горящего вещества в контейнер.
- Постепенно добавлять взвешивательные гири на платформу весов, чтобы достичь равновесия.
- Зафиксировать массу горящего вещества с точностью до миллиграммов.
Массу горящего вещества можно рассчитать, вычтя массу пустого контейнера из общей массы образца и контейнера. Результат позволит определить точную массу горящего вещества для проведения дальнейших расчетов или анализа.
Метод взвешивания является одним из наиболее точных методов определения массы горящего вещества и широко применяется в лабораторных условиях. Важно помнить о необходимости соблюдения правил работы с аналитическими весами и точности измерений, чтобы получить достоверные результаты.
Метод гравиметрического анализа

Основным принципом гравиметрического анализа является сохранение массы вещества во время химических реакций. При проведении анализа вещество смешивается с реагентом, который вызывает химическую реакцию. В результате этой реакции образуется новое вещество или осаждение, которое имеет другую массу.
Чтобы определить массу горящего вещества, необходимо провести ряд химических реакций и измерить изменение массы веществ после каждого шага. Измерение массы может быть выполнено с помощью весов или баланса.
Одним из наиболее распространенных методов гравиметрического анализа является метод осаждения. В этом методе вещество осаждается из раствора в виде твердого осадка, который затем можно взвесить. Масса осадка будет пропорциональна массе горящего вещества в исходном образце.
Другим методом гравиметрического анализа является метод титрования. В этом методе реагент, содержащий известное количество вещества, добавляется к образцу до тех пор, пока не будет достигнуто полное осаждение или нейтрализация. Затем масса добавленного вещества может быть измерена, и на основе этого можно определить массу горящего вещества.
Гравиметрический анализ является важным инструментом в химической лаборатории и используется для решения широкого спектра задач, включая определение содержания примесей в образцах, поиск концентрации вещества в растворе и определение состава сложных смесей.
Метод термического анализа
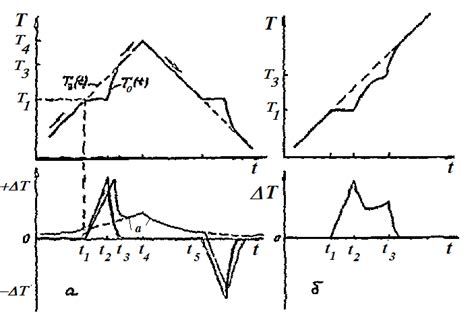
Основной принцип метода заключается в определении изменения температуры образца в зависимости от времени при его нагревании. При этом происходит испарение, деградация или реакция горючего вещества, и этот процесс сопровождается тепловым эффектом. Измеряя тепловые изменения, можно определить массу горящего вещества.
Термический анализ проводится с использованием специального оборудования, такого как термостаты, термобалансы и калориметры. Образец горючего вещества помещается в специальную камеру, которая нагревается с заданной скоростью. В процессе нагревания измеряются температура и тепловой поток, что позволяет определить изменение массы вещества.
Определение массы горящего вещества с использованием метода термического анализа широко применяется в различных областях, включая химическую промышленность, пищевую промышленность, фармацевтику и др. Этот метод позволяет получить точные и надежные результаты, что делает его неотъемлемой частью процесса анализа горючих веществ.
Формула расчета массы горящего вещества

Для определения массы горящего вещества можно использовать следующую формулу:
| Масса горящего вещества (мгв) | = | Масса образца (мо) - Масса несгоревшего остатка (мно) |
В данной формуле:
- Масса горящего вещества (мгв) - это величина, которую необходимо определить.
- Масса образца (мо) - это масса исходного вещества или материала, который был подвергнут горению.
- Масса несгоревшего остатка (мно) - это масса остаточного вещества после горения, которое не включается в расчет массы горящего вещества.
Для определения массы образца и массы несгоревшего остатка могут использоваться различные методы, в зависимости от конкретной ситуации и вещества. При проведении экспериментов важно быть внимательным и точным в измерениях, чтобы получить достоверные результаты.
Пример использования формулы

Давайте рассмотрим пример использования формулы для определения массы горящего вещества. Предположим, что у нас имеется девятьдесятый процентный раствор кислоты объемом 500 мл. Нам необходимо определить массу кислоты в этом растворе.
Для решения этой задачи мы можем использовать формулу:
Масса горящего вещества = Концентрация x Объем
В данном случае, концентрация кислоты равна 90% (или 0,9), а объем раствора равен 500 мл. Подставляя значения в формулу, получаем:
Масса горящего вещества = 0,9 x 500 мл = 450 г
Таким образом, масса кислоты в этом растворе составляет 450 г.
Используя данную формулу и данные о концентрации и объеме вещества, мы можем легко определить массу горящего вещества. Учитывайте, что эта формула применима и для других типов горящих веществ, не только кислот.
Важно: При работе с горючими веществами необходимо соблюдать все меры предосторожности и следовать инструкциям безопасности.