Определение молярной массы в химии является важным шагом для понимания и применения различных химических процессов. Молярная масса означает массу одного моля вещества и выражается в граммах на моль (г/моль). Зная молярную массу, можно определить количество вещества и произвести различные расчеты в химических реакциях.
Одним из способов определения молярной массы является использование таблицы Менделеева. Таблица Менделеева является структурированным справочником, в котором элементы упорядочены по атомному номеру, атомной массе и химическим свойствам. Каждый элемент таблицы содержит информацию о его символе, атомном номере, атомной массе и других химических свойствах.
Для определения молярной массы по таблице Менделеева необходимо учесть атомную массу каждого элемента в химической формуле соединения или молекулы. Атомные массы элементов пропорциональны их атомным номерам в таблице Менделеева. Например, атомный номер азота (N) равен 7, а атомная масса равна примерно 14 г/моль. Путем сложения атомных масс всех элементов в химической формуле можно найти молярную массу соединения в г/моль.
Молярная масса: определение и значение
Молярная масса позволяет определить, сколько граммов данного вещества содержится в одном моле. Такая информация необходима для проведения различных расчетов в химических реакциях: определения количества вещества, объемов реакционных смесей и других параметров.
Определить молярную массу можно с помощью таблицы Менделеева, где указана атомная масса каждого элемента. Для этого необходимо сложить массы атомов вещества, учитывая их количество в молекуле или соединении.
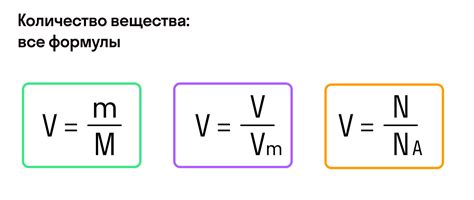
Зная молярную массу вещества, можно также определить его молярный объем при определенной температуре и давлении. Для этого необходимо использовать уравнение состояния и идеальный газовый закон.
Молярная масса является фундаментальным показателем в химии и используется во множестве различных расчетов и формул. Правильное определение молярной массы позволяет точно проводить расчеты химических реакций и свойств вещества, что является важным в химической науке и промышленности.
Что такое молярная масса?

Зная молярную массу, можно определить массу данного количества вещества в граммах или в килограммах. Для этого нужно умножить количество молей на молярную массу. Например, если у нас имеется 2 моля вещества, молярная масса которого равна 10 г/моль, то масса этого вещества будет 20 г (2 моля × 10 г/моль = 20 г).
Как определить молярную массу? Методы расчета

Существует несколько методов расчета молярной массы, в зависимости от доступности информации о химическом соединении. Рассмотрим некоторые из них:
1. Расчет молярной массы из атомных масс
Самый простой способ определить молярную массу - это использовать значения атомных масс элементов, представленные в таблице Менделеева. Для этого необходимо узнать количество каждого атома в соединении и умножить его на соответствующую атомную массу. Затем полученные значения сложить.
Например, для расчета молярной массы воды (H2O) необходимо взять атомную массу водорода (1 г/моль) и атомную массу кислорода (16 г/моль), умножить их на количество атомов в соединении (2 для водорода и 1 для кислорода) и сложить полученные значения: (1 г/моль * 2 атома) + (16 г/моль * 1 атом) = 18 г/моль.
2. Расчет молярной массы из процентного состава
Если известен процентный состав химического соединения, то можно воспользоваться формулой для расчета молярной массы. Для этого необходимо разделить процент содержания каждого элемента на его атомную массу и сложить полученные значения.
Например, если известно, что вещество состоит из 40% углерода, 6.7% водорода и 53.3% кислорода, то можно расчитать его молярную массу следующим образом: (40/12 г/моль) + (6.7/1 г/моль) + (53.3/16 г/моль) = 3.33 г/моль + 6.7 г/моль + 3.33 г/моль = 13.36 г/моль.
3. Расчет молярной массы из массы образца
Если известна масса химического соединения, то можно расчитать его молярную массу, используя формулу для расчета числа молей. Для этого необходимо разделить массу образца на его массу одного моля.
Например, если известно, что масса образца составляет 25 г, а химическое соединение представляет собой C6H12O6, то можно расчитать его молярную массу следующим образом: масса одного моля C6H12O6 (180 г/моль) исходя из уравнения массы их плотности (масса образца / масса одного моля) = 25 г / 180 г/моль = 0.14 моль/литр.
Таким образом, существует несколько методов расчета молярной массы вещества, в зависимости от доступности информации. Расчет по таблице Менделеева или по известному процентному составу являются самыми распространенными методами.
Таблица Менделеева и молярная масса химических элементов
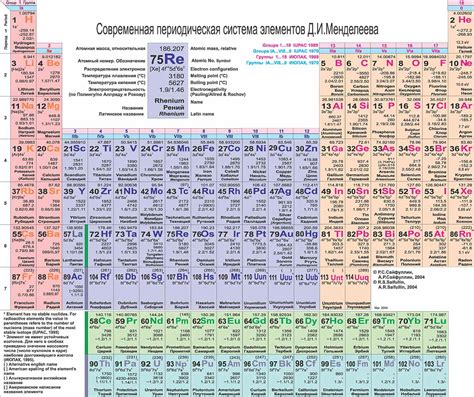
Периодическая система химических элементов, разработанная Дмитрием Ивановичем Менделеевым, представляет собой систематизированную таблицу, которая отражает все известные элементы в отсортированном порядке по их атомным номерам. В таблице Менделеева каждый элемент обозначается символом и содержит информацию о своей атомной массе, атомном номере и химических свойствах.
Молярная масса химического элемента является основным параметром, который позволяет определить его массу в граммах при переходе от количества вещества к массе. Молярная масса измеряется в граммах на моль и представляет собой сумму атомных масс всех атомов в молекуле элемента.
Таблица Менделеева является отличным справочником для определения молярной массы химических элементов. Она содержит информацию о точных значениях атомных масс элементов или их приближенном значении, если атомных масс точно не известно. Для определения молярной массы элемента из таблицы Менделеева необходимо найти его атомную массу, которая указывается под символом элемента, и выразить ее в граммах на моль.
Например, для определения молярной массы кислорода (O) из таблицы Менделеева необходимо найти его атомную массу, которая равна примерно 16 г/моль. Таким образом, молярная масса кислорода составляет примерно 16 г/моль.
Использование таблицы Менделеева для определения молярной массы химических элементов является важной задачей в химии. Знание молярной массы позволяет проводить расчеты и определять массу вещества при заданном количестве, а также выполнять другие химические операции.
Справочник по молярным массам известных веществ
| Вещество | Химический символ | Молярная масса (г/моль) |
|---|---|---|
| Водород | H | 1.008 |
| Кислород | O | 16.00 |
| Углерод | C | 12.01 |
| Азот | N | 14.01 |
| Фтор | F | 19.00 |
| Хлор | Cl | 35.45 |
| Бром | Br | 79.90 |
| Йод | I | 126.90 |
| Алюминий | Al | 26.98 |
| Железо | Fe | 55.85 |
Формула для расчета молярной массы соединения
Молярная масса соединения определяется с использованием таблицы Менделеева и формулы, которая учитывает все атомы и их относительные массы в составе соединения. Формула для расчета молярной массы соединения выглядит следующим образом:
- Найдите химическую формулу соединения.
- Определите количество атомов каждого элемента в формуле соединения.
- Найдите молярную массу каждого элемента по таблице Менделеева.
- Умножьте количество атомов каждого элемента на его молярную массу.
- Сложите полученные произведения, чтобы получить молярную массу соединения.
Например, для расчета молярной массы воды (H2O) сначала определяются молярные массы водорода (H) и кислорода (O) по таблице Менделеева. Затем умножают количество атомов каждого элемента (2 атома водорода и 1 атом кислорода) на их молярную массу и складывают полученные произведения. Таким образом, молярная масса воды равна сумме молярных масс водорода и кислорода.
Практический пример расчета молярной массы
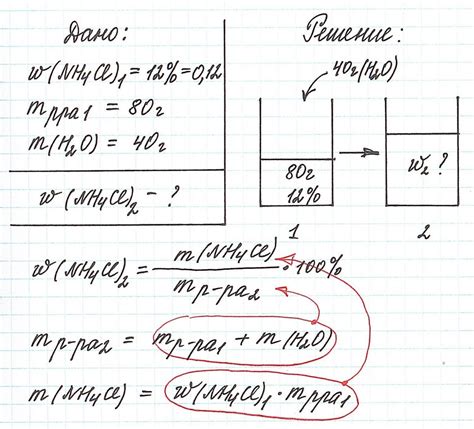
Для лучшего понимания процесса расчета молярной массы по таблице Менделеева рассмотрим следующий практический пример.
Допустим, у нас есть химическое соединение, представленное формулой: H2O.
В этом случае, мы имеем 2 атома водорода (H) и 1 атом кислорода (O).
Согласно таблице Менделеева, молярная масса водорода (H) составляет примерно 1 г/моль, а молярная масса кислорода (O) около 16 г/моль.
Чтобы рассчитать молярную массу H2O, нужно умножить число атомов каждого элемента на их молярную массу и сложить результаты.
Для водорода (H) получим: 2 атома * 1 г/моль = 2 г/моль.
Для кислорода (O) получим: 1 атом * 16 г/моль = 16 г/моль.
Таким образом, молярная масса H2O равна 2 г/моль + 16 г/моль = 18 г/моль.
Итак, молярная масса вещества H2O составляет 18 г/моль.
Такой пример позволяет лучше понять, как можно использовать таблицу Менделеева для расчета молярной массы химических соединений.