Молекулярный вес - один из важнейших параметров химического соединения, который определяет его состав и свойства. Знание молекулярного веса позволяет ученым и химикам лучше понимать структуру и реактивность вещества. Но как же узнать молекулярный вес?
Существуют различные методы и формулы, позволяющие определить молекулярный вес химического соединения. Один из самых простых и распространенных методов - это суммирование атомных масс атомов, составляющих молекулу. Для этого необходимо знать химическую формулу соединения и массы атомов его элементов.
При определении молекулярного веса химического соединения можно использовать также формулу количество (г) = молярная масса (г/моль) × количество вещества (моль). Таким образом, зная количество вещества и молярную массу, можно вычислить массу химического соединения в граммах. Этот метод особенно удобен при проведении химических расчетов и экспериментов.
Узнать молекулярный вес в химии - важный этап в изучении химических соединений. Знание молекулярного веса позволяет более глубоко понять особенности и свойства вещества, его возможные реакции и применение. Определение молекулярного веса может быть полезным и в промышленных областях, где необходимо контролировать качество и состав химических веществ.
Что такое молекулярный вес?

Молекулярный вес выражается в атомных массах имере указывает, сколько раз масса молекулы превышает массу одного атома углерода-12. Единицей измерения молекулярного веса является атомная массовая единица (аму), где 1 аму равна одной двенадцатой массы атома углерода-12.
| Величина | Обозначение |
|---|---|
| Относительная атомная масса | А |
| Массовое число | Z |
| Молекулярное число | N |
| Молекулярный вес | M = A * N |
Молекулярный вес помогает в определении структуры и свойств вещества, а также используется при проведении различных химических реакций, расчете количества реактивов и продуктов.
Вычисление молекулярного веса производится путем умножения относительной атомной массы каждого элемента в молекуле на количество атомов этого элемента и сложения всех полученных произведений.
Знание молекулярного веса позволяет химикам легко определить необходимое количество вещества для проведения определенной реакции и избежать ошибок в расчетах и экспериментах.
Зачем нужно знать молекулярный вес?

Во-первых, молекулярный вес позволяет определить количество атомов, присутствующих в молекуле вещества. Это особенно важно при проведении химических реакций, где точное соотношение реагентов и продуктов играет решающую роль.
Во-вторых, знание молекулярного веса позволяет рассчитать количество ионов или молекул вещества в заданном объеме или массе. Это полезно при проведении различных экспериментов и при подготовке растворов с определенной концентрацией.
Кроме того, молекулярный вес может использоваться для определения плотности вещества и для оценки его физических свойств, таких как температура кипения или смешиваемость с другими веществами.
Также молекулярный вес является важным параметром при проведении анализа состава вещества, так как можно сравнить полученный молекулярный вес с известными значениями и определить состав, чистоту и степень идентичности вещества.
Наконец, знание молекулярного веса может быть полезным при проведении биохимических и медицинских исследований, так как позволяет установить взаимодействия между различными соединениями и оценить их воздействие на организм.
- Определение соотношения реагентов и продуктов в химических реакциях.
- Расчет концентрации растворов и смесей веществ.
- Оценка физических свойств вещества.
- Анализ состава вещества.
- Биохимические и медицинские исследования.
Методы определения молекулярного веса
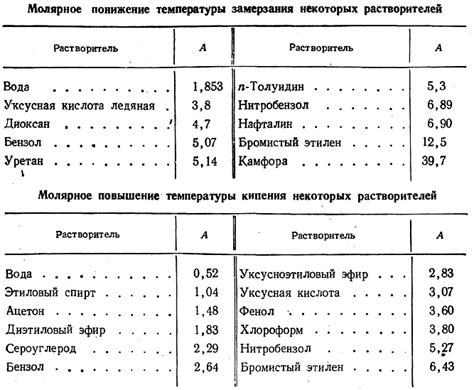
В химии существуют различные методы определения молекулярного веса вещества. Каждый из них основан на различных принципах и применяется в зависимости от конкретных условий и требуемой точности результата.
Газовая хроматография - один из наиболее распространенных методов определения молекулярного веса. Он основан на принципе разделения компонентов смеси и анализе времени их задержки на стационарной фазе.
Масс-спектрометрия - метод, основанный на разделении молекул вещества по массе и заряду, позволяющий определить массу отдельных ионов. По полученным данным можно рассчитать молекулярный вес вещества.
Осмотическое давление - метод, основанный на измерении давления, создаваемого полимерной молекулой в растворе. Измеряя это давление и зная концентрацию раствора, можно вычислить молекулярный вес полимера.
Электрофорез - метод, основанный на разделении заряженных частиц в электрическом поле. Молекулярный вес вещества можно определить по месту его задержки в геле или на специальном материале.
Это лишь несколько примеров методов определения молекулярного веса в химии. Каждый из этих методов имеет свои преимущества и ограничения, и выбор конкретного метода зависит от ряда факторов, таких как тип вещества, требуемая точность и доступность оборудования.
Химический анализ

Химический анализ включает в себя различные методы, такие как качественный анализ, который используется для определения наличия или отсутствия определенного химического вещества в образце, и количественный анализ, который определяет концентрацию или количество вещества в образце.
Существуют различные методы, используемые в химическом анализе, включая хроматографию, спектроскопию, электроанализ, гравиметрию и титрование. Каждый метод имеет свои сильные и слабые стороны и может быть применен для решения различных аналитических задач.
Важной частью химического анализа является также обработка и интерпретация данных. Чтобы получить точные и достоверные результаты анализа, необходимо правильно обработать и проанализировать полученные данные.
Химический анализ является неотъемлемой частью современной науки и технологии. Он позволяет исследовать и понимать молекулярную структуру вещества, определять его свойства и использовать в различных областях науки и промышленности.
В целом, химический анализ играет ключевую роль в расширении наших знаний о химии и содействует развитию новых материалов и технологий.
Масс-спектрометрия

Принцип масс-спектрометрии основан на разделении ионов по их массе и заряду в магнитном поле и детектировании полученных результатов. Процесс анализа включает несколько этапов:
1. Ионизация: вещество подвергается ионизации, при которой образуются ионы. Это может происходить различными способами, например, с помощью электронного пучка или лазерного излучения.
2. Разделение: ионы проходят через магнитное поле, где они разделяются по соотношению массы и заряда. В результате получается спектр ионов с разными массами.
3. Детектирование: полученный спектр ионов регистрируется детектором, который измеряет их число и интенсивность.
4. Анализ: на основе полученных данных строится масс-спектр, который представляет собой график, отражающий относительную массу ионов вещества и их интенсивность.
Использование масс-спектрометрии позволяет определить молекулярный вес соединения с высокой точностью. С помощью этого метода также возможно исследование структуры молекулы, выявление примесей и даже определение изотопного состава вещества.
Масс-спектрометрия является одним из наиболее точных и надежных методов анализа, используемых в химии и биологии. Она находит широкое применение в различных областях, включая фармацевтику, пищевую промышленность, медицину и научные исследования.
Газовая хроматография

ГХ состоит из двух основных частей: колонки и детектора. Колонка представляет собой тонкую трубку, внутри которой происходит разделение компонентов смеси. Детектор служит для регистрации проходящих через него компонентов. Для ГХ часто используются различные типы детекторов, такие как теплопроводящие, флюоресцентные и масс-спектрометрические.
Процесс газовой хроматографии начинается с ввода образца в систему. Образец может быть газом или жидкостью, который подвергается испарению перед вводом в систему. Затем образец вводится в колонку, где происходит разделение компонентов смеси.
Важной составляющей ГХ является носительный газ, который приводит разделенные компоненты к детектору. Носительный газ выбирается таким образом, чтобы он не реагировал с компонентами смеси и пропорционально переносил их к детектору.
По мере прохождения компонентов через колонку, они взаимодействуют со стационарной фазой, содержащейся внутри колонки. Такие взаимодействия могут быть различными и влиять на скорость движения компонентов. Более "сильное" взаимодействие означает медленную скорость движения, а "слабое" - быструю скорость движения.
В результате разделения компонентов смеси на различные времена удерживания их можно детектировать. Детектор регистрирует проходящие через него компоненты и создает график, известный как хроматограмма. Хроматограмма представляет собой пиковую диаграмму, где каждый пик соответствует определенному компоненту смеси.
Газовая хроматография является одним из наиболее точных и чувствительных методов анализа в химии. Он широко применяется в различных областях, таких как фармацевтика, пищевая промышленность, нефтяная промышленность и многие другие.
Формулы для расчета молекулярного веса
Существуют различные формулы для расчета молекулярного веса в химии.
1. Простая формула
Молекулярный вес (МВ) = сумма масс атомов в молекуле
Например, для воды (H2O) масса водорода (H) равна 1, а масса кислорода (O) равна 16. Таким образом, МВ воды = 2 * 1 + 16 = 18.
2. Формула с использованием химической формулы
МВ = (масса атома 1 * количество атомов 1) + (масса атома 2 * количество атомов 2) + ...
Например, для глюкозы (C6H12O6) масса атома углерода (C) равна 12, масса атома водорода (H) равна 1, а масса атома кислорода (O) равна 16. Таким образом, МВ глюкозы = (12 * 6) + (1 * 12) + (16 * 6) = 180.
3. Формула с использованием структурной формулы
МВ = (Масса атома 1 * количество атомов 1 в молекуле 1) + (Масса атома 2 * количество атомов 2 в молекуле 2) + ...
Например, для метана (CH4) масса атома углерода (C) равна 12, масса атома водорода (H) равна 1. Таким образом, МВ метана = (12 * 1) + (1 * 4) = 16.
Правильное определение молекулярного веса химического вещества является ключевым моментом в химических расчетах и может быть полезно для понимания структуры и свойств вещества.
Суммарная масса атомов
Для определения суммарной массы атомов в молекуле используется периодическая таблица элементов. Каждый элемент в периодической таблице имеет указанную атомную массу. Атомная масса представляет собой массу одного атома данного элемента.
Для определения суммарной массы атомов в молекуле необходимо умножить атомную массу каждого атома на его количество в молекуле и затем просуммировать полученные значения.
| Элемент | Атомная масса (г/моль) | Количество атомов | Суммарная масса (г/моль) |
|---|---|---|---|
| Углерод (C) | 12.01 | 2 | 24.02 |
| Кислород (O) | 16.00 | 1 | 16.00 |
| Водород (H) | 1.01 | 4 | 4.04 |
Например, в молекуле этилового спирта (C2H5OH), суммарная масса атомов можно рассчитать следующим образом:
Суммарная масса = (масса атома углерода × количество атомов углерода) + (масса атома водорода × количество атомов водорода) + (масса атома кислорода × количество атомов кислорода)
= (12.01 г/моль × 2) + (1.01 г/моль × 5) + (16.00 г/моль × 1)
= 24.02 г/моль + 5.05 г/моль + 16.00 г/моль
= 45.07 г/моль
Таким образом, суммарная масса атомов в молекуле этилового спирта составляет 45.07 г/моль.
Расчет суммарной массы атомов позволяет определить молекулярный вес вещества, что является важной характеристикой в химии и используется в различных расчетах и реакциях.