Определение молекулярной массы вещества является важным аспектом изучения химии в 8 классе. Молекулярная масса позволяет узнать, сколько атомов содержится в одной молекуле вещества. Это полезная информация, которая помогает в понимании химических реакций и взаимодействий.
Существуют различные методы для определения молекулярной массы вещества, но в данной статье мы рассмотрим самый простой из них. Для начала, необходимо знать количество и тип атомов, из которых состоит молекула вещества. Эту информацию можно найти в химической формуле вещества.
После того, как мы определили химическую формулу вещества, можно приступать к вычислению молекулярной массы. Для этого необходимо найти атомные массы каждого атома, участвующего в реакции, и сложить их вместе. Например, если вещество состоит из атомов углерода, водорода и кислорода, то нужно найти атомные массы каждого из этих элементов и сложить их вместе.
Итак, определение молекулярной массы вещества в химии для 8 класса является несложной задачей, если у вас есть химическая формула и доступ к справочной литературе с атомными массами элементов. Следуя простому методу, описанному выше, вы сможете легко определить молекулярную массу вещества и углубить свои знания в области химии.
Как определить молекулярную массу вещества
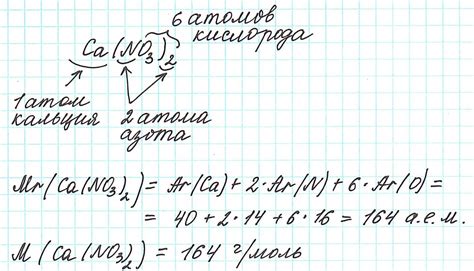
Существует несколько способов определения молекулярной массы вещества. Один из простых способов - использование таблицы молекулярных масс химических элементов. В таблице указаны массы атомов различных элементов в атомных единицах - аму.
Для определения молекулярной массы вещества необходимо:
- Разложить формулу вещества на отдельные атомы.
- Посчитать количество каждого атома в молекуле.
- Умножить массу каждого атома на его количество и сложить полученные значения.
Рассмотрим пример: молекулярная формула вещества - Н2О (вода).
Вода состоит из двух атомов водорода (Н) и одного атома кислорода (О). Используя таблицу молекулярных масс, находим, что масса атома водорода составляет 1 аму, а масса атома кислорода - 16 аму.
Умножаем массу атома водорода на количество атомов (2) и получаем 2 аму. Затем умножаем массу атома кислорода на количество атомов (1) и получаем 16 аму.
Складываем полученные значения: 2 аму + 16 аму = 18 аму. Таким образом, молекулярная масса воды равна 18 аму.
Таким же образом можно определить молекулярную массу других веществ, используя таблицу молекулярных масс химических элементов.
Зная молекулярную массу вещества, можно провести различные расчеты, например, определить массу вещества, количество молекул вещества и т.д.
Понятие молекулярной массы в химии
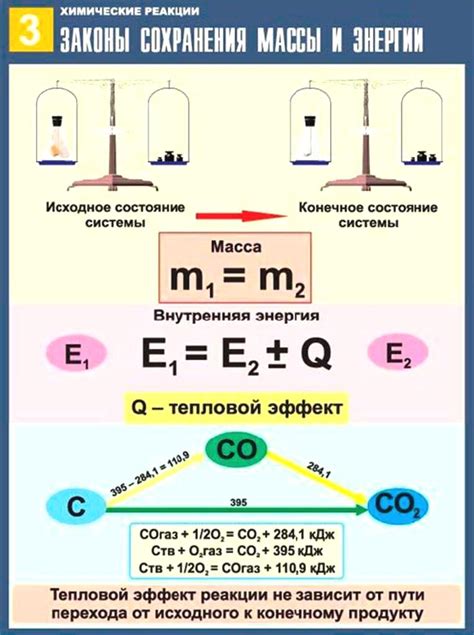
Расчет молекулярной массы осуществляется с помощью периодической системы элементов. В периодической системе указаны атомные массы элементов, выраженные в атомных единицах. Для определения молекулярной массы нужно узнать, сколько атомов каждого элемента содержится в молекуле вещества и перемножить эти числа на соответствующие атомные массы.
Для наглядности работы с молекулярными массами можно составить таблицу, где в первом столбце записаны химические формулы веществ, во втором - числа атомов каждого элемента, а в третьем - атомные массы элементов. Путем перемножения чисел атомов и атомных масс каждого элемента и последующего сложения полученных значений можно рассчитать молекулярную массу вещества.
| Химическая формула | Число атомов каждого элемента | Атомная масса элемента (у) |
|---|---|---|
| H2O | 2 | 1 |
| CO2 | 1 | 12 |
| C6H12O6 | 6 | 12 |
Например, для воды (H2O) молекулярная масса будет равна: (2 * 1) + 16 = 18 (у). Для углекислого газа (CO2) молекулярная масса будет равна: (1 * 12) + (2 * 16) = 44 (у). Данные значения позволяют определить массу одной молекулы вещества.
Таким образом, понятие молекулярной массы в химии является важным инструментом для определения состава и количества вещества в химических реакциях. Расчет молекулярной массы помогает понять, какие элементы и в каких количествах входят в молекулу вещества, что является основой для дальнейшего изучения химических процессов и закономерностей.
Простой способ определения молекулярной массы

Существует простой способ определения молекулярной массы: использование периодической системы элементов. В периодической системе элементов указана атомная масса каждого элемента. Атомная масса представляет собой массу атома элемента в атомных единицах.
Чтобы определить молекулярную массу вещества, нужно сложить атомные массы всех атомов, составляющих молекулу. Например, если мы имеем молекулу воды (H2O), то нужно сложить массу двух атомов водорода (H) и массу одного атома кислорода (O).
Важно помнить, что молекулярная масса измеряется в атомных массовых единицах (аму). Она также может быть выражена в граммах на моль (г/моль).
Таким образом, использование простого метода определения молекулярной массы с помощью периодической системы элементов позволяет узнать массу молекулы вещества и проводить различные химические расчеты.
Как провести экспериментальный расчет

Для проведения экспериментального расчета молекулярной массы вещества в химии для 8 класса потребуются следующие материалы и оборудование:
| Материалы | Оборудование |
|---|---|
| Вещество, масса которого известна | Весы |
| Вещество, массу которого нужно определить | Пробирки |
| Вода | Шпатель |
| Линейка | Маркер |
Процесс экспериментального расчета молекулярной массы вещества можно разделить на следующие шаги:
- Подготовьте две пробирки: одну для вещества, массу которого нужно определить, и другую для вещества, массу которого известна.
- С помощью шпателя добавьте небольшое количество обоих веществ в соответствующие пробирки.
- Используя весы, измерьте массу каждой пробирки.
- Добавьте воду в каждую пробирку, чтобы заполнить их на 1/3 объема.
- Тщательно перемешайте содержимое каждой пробирки.
- С помощью линейки определите изменение уровня жидкости в пробирках.
Для расчета молекулярной массы вещества используйте следующую формулу:
Молекулярная масса неизвестного вещества = (Молекулярная масса известного вещества * изменение уровня жидкости в пробирке с неизвестным веществом) / изменение уровня жидкости в пробирке с известным веществом.
Таким образом, проведя экспериментальный расчет, вы сможете определить молекулярную массу вещества в химии для 8 класса. Этот простой способ поможет вам лучше понять молекулярную структуру веществ и их химические свойства.
Примеры определения молекулярной массы

Для определения молекулярной массы вещества можно использовать простой подход, основанный на сумме атомных масс элементов, составляющих молекулу. Ниже приведены несколько примеров, которые помогут вам лучше понять этот процесс.
Пример 1:
Рассмотрим молекулу воды (H2O). Вода состоит из двух атомов водорода и одного атома кислорода. Получим сумму атомных масс компонентов:
- Атом водорода (H) имеет молекулярную массу 1 г/моль (1u).
- Атом кислорода (O) имеет молекулярную массу 16 г/моль (16u).
Суммируя молекулярные массы элементов, получим молекулярную массу воды:
- (2 * 1) + 16 = 2 + 16 = 18 г/моль (18u).
Пример 2:
Рассмотрим молекулу диоксида углерода (CO2). Диоксид углерода состоит из одного атома углерода и двух атомов кислорода. Получим сумму атомных масс компонентов:
- Атом углерода (C) имеет молекулярную массу 12 г/моль (12u).
- Атом кислорода (O) имеет молекулярную массу 16 г/моль (16u).
Суммируя молекулярные массы элементов, получим молекулярную массу диоксида углерода:
- 12 + (2 * 16) = 12 + 32 = 44 г/моль (44u).
Пример 3:
Рассмотрим молекулу метана (CH4). Метан состоит из одного атома углерода и четырех атомов водорода. Получим сумму атомных масс компонентов:
- Атом углерода (C) имеет молекулярную массу 12 г/моль (12u).
- Атом водорода (H) имеет молекулярную массу 1 г/моль (1u).
Суммируя молекулярные массы элементов, получим молекулярную массу метана:
- 12 + (4 * 1) = 12 + 4 = 16 г/моль (16u).
Таким образом, зная молекулярные массы элементов и их количество в молекуле, можно определить молекулярную массу вещества. Этот простой метод может быть полезен при изучении химии для 8 класса.