Для людей, которые интересуются химией и физикой, вопрос о количестве протонов в атоме является одним из важных. Протоны - это основные частицы, составляющие ядро атома. Понимание, сколько протонов содержится в атоме, помогает установить его идентичность и характеристики. Хотя протоны нельзя увидеть невооруженным глазом, существует несколько простых шагов, которые позволяют определить число этих частиц.
Первым шагом в определении количества протонов в атоме является поиск элемента в таблице химических элементов. В таблице будут указаны символы элементов, их атомные номера и атомные массы. Атомный номер - это число, которое показывает количество протонов в ядре атома. Например, для элемента водород, атомный номер равен 1, что означает, что в атоме водорода содержится 1 протон. Таким образом, нахождение атомного номера элемента позволяет определить количество протонов в его атоме.
Однако, если вам необходимо определить количество протонов в определенном атоме, а не в элементе в целом, есть еще одна возможность. Массовое число элемента, указанное в таблице, представляет собой сумму протонов и нейтронов в ядре. Учитывая, что протоны имеют положительный заряд, а нейтроны не имеют зарядового значения, разница между массовым числом и атомным номером элемента позволяет определить количество нейтронов. Используя это знание, вы можете легко рассчитать количество протонов, вычитая количество нейтронов из массового числа элемента.
Понятие протона

Протоны вместе с нейтронами составляют ядро атома, вокруг которого перемещаются электроны. Общее число протонов в атоме называется атомным номером и определяет его химические свойства и положение в периодической системе. Например, атом водорода имеет один протон, а атом углерода имеет шесть протонов.
Протон был открыт в 1918 году исследователем Эрнестом Резерфордом. В 1932 году Джеймс Чедвик вместе с коллегами установили, что протон – основная составляющая атомного ядра.
Что такое протон и как он связан с атомом
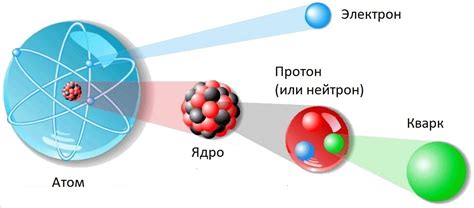
Протоны связаны с атомом через электромагнитные силы. Они существуют вместе с нейтронами в атомных ядрах и образуют вместе с ними протонную материю. Протоны также обладают электрическим зарядом, который компенсируется отрицательно заряженными электронами, находящимися на внешнем электронном облаке атома.
Количество протонов в атоме определяет его атомный номер и определяет его химические свойства. Например, у атома водорода есть один протон, а у атома гелия - два протона. Количество протонов также определяет массовый номер атома, так как оно примерно равно сумме протонов и нейтронов в ядре.
Протоны являются неотъемлемой частью атомной структуры и играют важную роль во всей химии и физике. Изучение и понимание количества протонов в атоме позволяет уточнить его свойства и установить его место в периодической системе элементов.
Значение протонов для понимания строения атомов

Протоны обладают положительным электрическим зарядом и находятся в ядре атома вместе с нейтронами. Количество протонов определяет химические и физические свойства элемента и является основой для классификации атомов в таблице химических элементов.
В таблице химических элементов, каждый элемент обозначается символом и числом. Символ представляет собой обозначение элемента на латинском языке, а число обозначает количество протонов в атоме этого элемента, известное как атомный номер.
| Символ элемента | Атомный номер |
|---|---|
| H | 1 |
| He | 2 |
| Li | 3 |
| Be | 4 |
| B | 5 |
Например, элемент с символом H имеет атомный номер 1, что означает наличие одного протона в ядре атома. Число протонов также определяет заряд ядра, поскольку протоны имеют положительный заряд, а электроны находятся в облаке вокруг ядра и имеют отрицательный заряд.
Изучение количества протонов в атоме помогает в понимании многих явлений, связанных с химией и физикой. Оно позволяет определить электрическую зарядность, массу и другие характеристики атомов, а также понять, как взаимодействуют атомы между собой и с другими веществами.
Методы определения количества протонов

Существует несколько методов, позволяющих определить количество протонов в атоме. Рассмотрим некоторые из них:
- Масс-спектрометрия: данный метод основывается на измерении массы атомов. Путем анализа масс-спектра можно определить массу и заряд атому. Количество протонов будет равно заряду атома.
- Химический анализ: данный метод основывается на изучении химических свойств атома. При изучении реакций атома с другими веществами можно определить его заряд. Количество протонов будет равно заряду атома.
- Электронная спектроскопия: данный метод основывается на изучении поглощения и испускания атомами электромагнитного излучения. По спектру поглощения или испускания атома можно определить его энергетические уровни и, соответственно, количество протонов.
- Рентгеновская флуоресценция: данный метод основывается на возбуждении атов рентгеновским излучением. По спектру рентгеновской флуоресценции можно определить химический состав атома и тем самым количество протонов.
Каждый из этих методов имеет свои особенности и применяется в различных научных исследованиях для определения количества протонов в атоме. Выбор метода зависит от особенностей рассматриваемой системы и целей исследования.
Использование периодической таблицы элементов
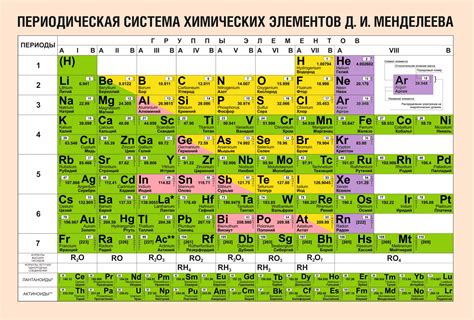
Атомный номер элемента в периодической таблице указывает на количество протонов в атоме данного элемента. Например, углерод имеет атомный номер 6, что означает наличие 6 протонов в его атоме.
Для определения количества протонов в атоме нужно найти элемент в периодической таблице и ознакомиться с его атомным номером. Атомный номер обычно указывается над символом элемента.
Важно заметить, что атомный номер также указывает на количество электронов в атоме при атоме в нейтральном состоянии. Это объясняет, почему число электронов в атоме также часто указывается в периодической таблице.
Использование периодической таблицы элементов позволяет легко и быстро определить количество протонов в атоме и расширяет наши знания о химических элементах.
Массовое число и атомное число
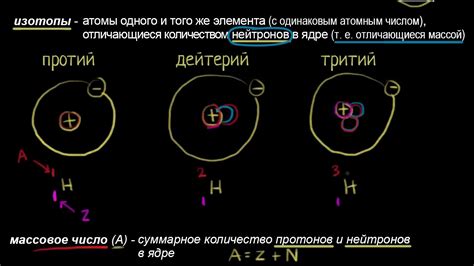
Атомное число - это количество протонов в атоме. Оно обозначается символом Z. Атомное число определяет химические свойства элемента и его положение в периодической таблице Менделеева.
Массовое число и атомное число являются основными характеристиками атома и позволяют его идентифицировать. Кроме того, они определяют электрический заряд атома и количество электронов, находящихся на его внешней оболочке.
Эксперименты и измерения

Определение количества протонов в атоме осуществляется с помощью различных физических экспериментов и измерений. Здесь приведены несколько основных методов, используемых в научных исследованиях.
| Метод | Описание |
|---|---|
| Масс-спектрометрия | Этот метод основан на разделении ионов по их массе и измерении их заряда. Ионы, имеющие одинаковую массу, но разную зарядность, могут быть разделены и обнаружены на детекторе. Измерение заряда и массы иона позволяет определить количество протонов. |
| Электростатическое измерение | Этот метод основан на измерении электрического заряда атома с помощью электростатических сил. Известная сила, действующая на атом с известным зарядом, позволяет определить заряд атома и, следовательно, количество протонов в нем. |
| Ядерные эксперименты | Ядерные эксперименты, такие как рассеяние и реакции с участием элементарных частиц, позволяют изучать строение атомного ядра и определить количество протонов. Анализ результатов этих экспериментов позволяет получить информацию о заряде и массе ядра и, следовательно, о количестве протонов. |
Эти методы позволяют ученым определить количество протонов в атоме с высокой точностью и проводить дальнейшие исследования в области физики и химии.
Измерение массы элемента

Масса элемента измеряется в атомных единицах массы, которые обычно обозначаются amu. Одна атомная единица массы равна примерно массе одного протона или нейтрона.
Существуют различные методы измерения массы элементов. Одним из наиболее распространенных является использование масс-спектрометра. В масс-спектрометре атомы элемента превращаются в ионы и ускоряются в магнитном поле. Затем ионы разделяются по их массе и проходят через детектор, который регистрирует количество ионо-токов разных масс. По результатам измерений можно определить массу или относительную массу элемента.
Другим методом измерения массы элемента является использование химических методов. Например, для определения массы углерода можно ввести известное количество углерода в реакцию с известным количеством других веществ и затем измерить массу образовавшегося продукта. Зная количество углерода, которое участвовало в реакции, и массу продукта, можно вычислить массу элемента.
Измерение массы элемента является важным шагом в определении количества протонов в атоме. Зная массу элемента и массу протона, можно вычислить количество протонов в атоме по формуле:
количество протонов = масса элемента / масса протона
Таким образом, измерение массы элемента играет ключевую роль в определении его строения и свойств.