Электролиты - это вещества, которые могут проводить электрический ток. Для химиков и студентов химической науки особенно важно определить, является ли данное вещество электролитом или нет. Как же это сделать? В этой статье мы расскажем о нескольких полезных советах, которые помогут вам определить электролиты и разобраться в их свойствах.
Первым шагом при определении электролитов является изучение химической формулы вещества. Часто электролитами являются соли, кислоты и щелочи, но они могут присутствовать и в других веществах. Если в формуле вещества присутствуют ионы (атомы с положительным или отрицательным зарядом), это может указывать на его электролитность. Однако необходимо учитывать, что не все вещества с ионами являются электролитами. Некоторые вещества могут содержать ионы, но при этом не проводить электрический ток.
Один из способов определить электролитность вещества - проведение электролиза. Электролиз представляет собой процесс разложения вещества под действием электрического тока. Если в результате электролиза в веществе образуются ионы и электроды начинают выделять газы или наблюдаются химические реакции, это свидетельствует о наличии электролита. Однако электролиз может быть сложным и опасным процессом, поэтому его следует проводить только под руководством опытных химиков.
Значение электролитов в химии
Электролиты используются в электрохимии для проведения электролиза, гальванических элементов и аккумуляторов. Они также необходимы для батарей, электролитических конденсаторов и других устройств энергетики.
В аналитической химии электролиты используются для проведения различных химических анализов, например, для определения содержания ионов в растворах. Ионы электролитов также могут быть использованы в химических реакциях для образования осадков или комплексных соединений.
В медицине электролиты играют важную роль в поддержании нормального функционирования организма. Они необходимы для поддержания внутриклеточного и межклеточного равновесия, регуляции объема жидкости, передачи нервных импульсов и других биологических процессов.
Электролиты также используются в пищевой промышленности, косметологии, фармацевтике и других отраслях, где они выполняют различные функции, например, регулируют кислотно-щелочной баланс или служат консервантами.
Определение электролитов важно для понимания химических свойств веществ и их влияния на окружающую среду и организмы. Знание о природе и поведении электролитов также позволяет разрабатывать новые материалы, процессы и технологии, которые могут быть полезны в науке, промышленности и медицине.
Различные виды электролитов
В химии существуют различные виды электролитов, каждый из которых имеет свои уникальные свойства и характеристики. Они классифицируются в зависимости от ионной проводимости и химической структуры.
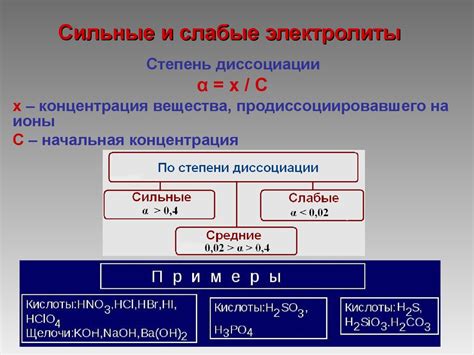
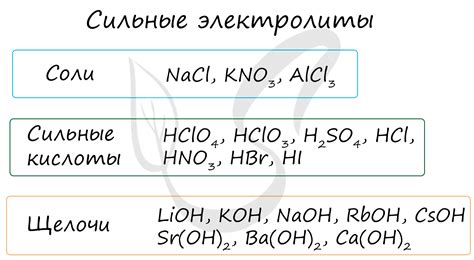
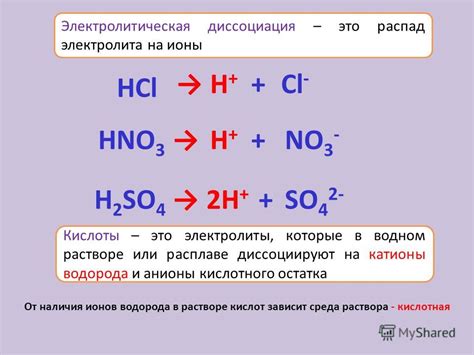
Одним из самых распространенных типов электролитов являются сильные электролиты. Они полностью или почти полностью диссоциируют в растворе на ионы и обладают высокой ионной проводимостью. Примерами сильных электролитов являются соли, кислоты и щелочи. Они играют важную роль во многих химических реакциях и процессах, таких как электролиз и электрохимические реакции.
Слабые электролиты, в отличие от сильных, не полностью диссоциируют в растворе и существуют как ионы и молекулы. Они обладают низкой ионной проводимостью и не являются такими активными в химических реакциях. Примерами слабых электролитов являются некоторые кислоты, основания и соли. Они находят применение в различных областях, включая фармацевтику и аналитическую химию.
Еще одним типом электролитов являются нейтральные электролиты. Они не обладают ни положительным, ни отрицательным зарядом. Примерами нейтральных электролитов являются некоторые молекулярные соединения и вещества. Невозможно их разделить на ионы, поскольку они не обладают зарядом и не диссоциируют в растворе.
| Тип электролита | Примеры |
|---|---|
| Сильные электролиты | Соли, кислоты, щелочи |
| Слабые электролиты | Некоторые кислоты, основания, соли |
| Нейтральные электролиты | Некоторые молекулярные соединения и вещества |
Понимание различных видов электролитов важно для понимания основных принципов химии и применения электролитов в различных областях. Это поможет определить их роль и функцию в химических реакциях и процессах.
Как определить наличие электролитов в растворе
- Проводимость раствора: одним из основных свойств электролитов является их способность проводить электрический ток. Для измерения проводимости раствора используются специальные устройства - проводимостиметры.
- Использование индикаторов: некоторые вещества, называемые индикаторами, могут изменять свой цвет или другие свойства в зависимости от наличия электролитов в растворе. Их использование позволяет косвенно определить наличие электролитов.
Изучение свойств электролитов важно не только для понимания химических процессов, но и для применения их в различных областях науки и техники, таких как электрохимия, биохимия, аналитическая химия и другие.
Методы определения электролитов

Один из самых простых методов - метод электропроводности. Суть метода заключается в измерении электрической проводимости раствора. Если раствор обладает высокой проводимостью, то это может означать наличие электролитов.
Другим методом является метод электрохимического анализа. Он основан на измерении электрических свойств анализируемого раствора с использованием электродов. Если при подключении электрода происходит реакция, которая приводит к изменению электрических параметров, то это может указывать на присутствие электролитов.
Также существует метод нейтрализации, основанный на реакции между кислотами и щелочами. При нейтрализации происходит ионный обмен, который может указывать на наличие электролитов.
| Метод | Описание |
|---|---|
| Метод электропроводности | Раствор с высокой проводимостью может содержать электролиты |
| Метод электрохимического анализа | Анализирование электрических свойств раствора с использованием электродов |
| Метод нейтрализации | Реакция между кислотами и щелочами может указывать на наличие электролитов |
Выбор метода определения электролитов зависит от конкретной ситуации и требований исследования. Кроме того, результаты определения электролитов могут быть использованы для проведения дальнейших химических исследований и анализа.
Полезные советы по определению электролитов
Вот несколько полезных советов, которые помогут вам определить электролиты:
| Совет | Описание |
| 1. | Проверьте растворимость вещества в воде. Если вещество растворяется и образует раствор, то оно скорее всего является электролитом. Например, NaCl – это ионный соединение и диссоциирует в растворе. |
| 2. | Проведите электрическую проводимость тестом. Электролиты проводят электрический ток, поэтому, если раствор вещества проводит ток, это говорит о наличии ионов. |
| 3. | Обратите внимание на состав вещества. Кислоты и основания являются электролитами, так как содержат ионы H+ и OH-. Некоторые металлы и соли также образуют ионы и являются электролитами. |
| 4. | Проанализируйте результаты реакций с другими веществами. Если вещество образует осадок или газ при добавлении другого вещества, это может указывать на наличие ионов и, следовательно, на электролитность. |
| 5. | Воспользуйтесь химическими методами определения электролитов, такими как титрование. Титрование позволяет определить концентрацию ионов в растворе и посчитать ионную силу. |
Используя эти полезные советы, вы сможете более точно определить электролиты и глубже понять их свойства и реакционную способность.