Концентрация раствора – важное понятие в химии, которое позволяет определить количество растворенного вещества в определенном объеме раствора. В основе концентрации лежит соотношение массы растворенного вещества к объему растворителя.
Измерение концентрации раствора производится с использованием специальных инструментов, таких как весы и мерные колбы. Обычно концентрация выражается в граммах растворенного вещества на 1 литр раствора или в процентах.
Величина концентрации раствора имеет большое значение при проведении химических экспериментов и производственных процессов. Она позволяет контролировать пропорции веществ в растворе и определить его свойства и реактивность.
Для расчета концентрации раствора необходимо знать массу растворенного вещества, объем раствора и плотность раствора. Существует несколько способов расчета концентрации, включая массовую, молярную и объемную концентрации.
Что такое концентрация раствора
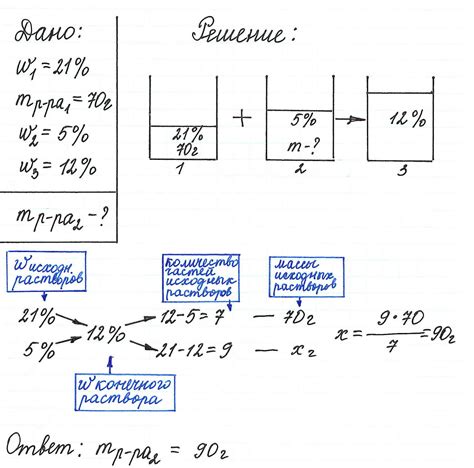
Массовая доля показывает, сколько граммов растворенного вещества содержится в 100 граммах раствора. Она вычисляется путем деления массы растворенного вещества на массу раствора и умножения на 100%.
Молярность - это количество молей растворенного вещества в 1 литре раствора. Она рассчитывается путем деления количества растворенного вещества (в молях) на объем раствора (в литрах).
Объемная доля указывает, сколько объемных единиц растворенного вещества содержится в 100 объемных единицах раствора. Она вычисляется путем деления объема растворенного вещества на объем раствора и умножения на 100%.
Концентрация раствора играет важную роль в химии, так как она позволяет определить, насколько насыщен раствор, а также оценить его химические свойства и применение.
Определение концентрации раствора в химии

Концентрация раствора может быть выражена различными способами. Наиболее распространенными способами измерения концентрации являются массовая и мольная концентрации.
Массовая концентрация определяется как отношение массы растворенного вещества к объему раствора. Она выражается в граммах на литр (г/л) и обозначается символом "с". Формула для расчета массовой концентрации:
c = m/V
где c - массовая концентрация, m - масса растворенного вещества, V - объем раствора.
Мольная концентрация определяется как отношение количества вещества (в молях) к объему раствора. Она выражается в молях на литр (М) и обозначается символом "С". Формула для расчета мольной концентрации:
C = n/V
где C - мольная концентрация, n - количество вещества, V - объем раствора.
Определение концентрации раствора может проводиться экспериментально с помощью методов измерения массы растворенного вещества или количества вещества. Существуют также методы расчета концентрации на основе данных о массе и объеме раствора.
Знание концентрации раствора важно при проведении химических реакций, анализе и синтезе веществ. Правильное определение концентрации раствора позволяет избежать ошибок при проведении химических экспериментов и обеспечивает получение точных результатов.
Методы измерения концентрации раствора

Для определения концентрации раствора существуют различные методы. Рассмотрим несколько из них:
| Метод | Описание |
|---|---|
| Гравиметрический метод | Этот метод основан на измерении массы сухого остатка после испарения раствора. Путем высушивания и взвешивания остатка можно определить его массу и, соответственно, концентрацию раствора. |
| Титриметрический метод | Титриметрический метод используется для измерения концентрации раствора путем добавления известного реактива и определения его точного объема, необходимого для полного реагирования с исследуемым раствором. |
| Спектрофотометрический метод | Спектрофотометрический метод основан на измерении поглощения света образцом раствора. Путем анализа изменения интенсивности поглощенного света можно определить концентрацию раствора. |
| Электрохимический метод | Электрохимический метод состоит в определении концентрации раствора с помощью электрических характеристик, таких как потенциал и проводимость. Это позволяет определить концентрацию ионов в растворе. |
Каждый из этих методов имеет свои преимущества и ограничения, и выбор метода зависит от химической системы и требуемой точности измерения.
Гравиметрический метод измерения концентрации раствора

Принцип гравиметрического метода заключается в том, что вещество, находящееся в растворе, может быть образовано в виде твердого осадка при реакции с присутствующим в растворе реагентом. Масса осадка определяется с помощью взвешивания, и по ней можно определить концентрацию вещества в растворе.
Для измерения концентрации раствора с использованием гравиметрического метода необходимо:
- Подобрать реагент, который образует твердый осадок с веществом, концентрацию которого нужно измерить.
- Провести реакцию, позволяющую образовать твердый осадок.
- Отфильтровать осадок и высушить его.
- Взвесить полученный осадок и записать его массу.
- По полученной массе осадка и стехиометрическим соотношениям между веществами определить концентрацию вещества в растворе.
Гравиметрический метод измерения концентрации раствора широко применяется в химическом анализе. Он позволяет получать точные результаты и часто используется для определения содержания различных элементов и соединений в растворах, например, для измерения содержания солей, металлов, кислот и оснований.
Весовой метод измерения концентрации раствора
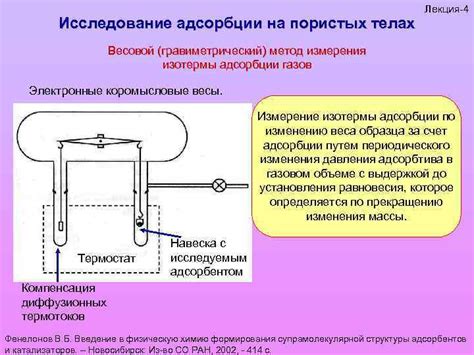
Для проведения весового метода измерения концентрации раствора необходимо:
- приготовить раствор заданной концентрации;
- перевесить определенный объем раствора;
- определить изменение массы раствора.
Измерение массы раствора производится с помощью аналитической весовой вилки или аналитических весов. Эти приборы позволяют определить массу раствора с высокой точностью.
После измерения массы раствора можно рассчитать его концентрацию, используя следующую формулу:
C = Δm / V
где C - концентрация раствора, Δm - изменение массы раствора, V - объем раствора.
Весовой метод измерения концентрации раствора является достаточно простым и точным. Он широко используется в химических лабораториях для проведения различных экспериментов и исследований.
Расчет концентрации раствора
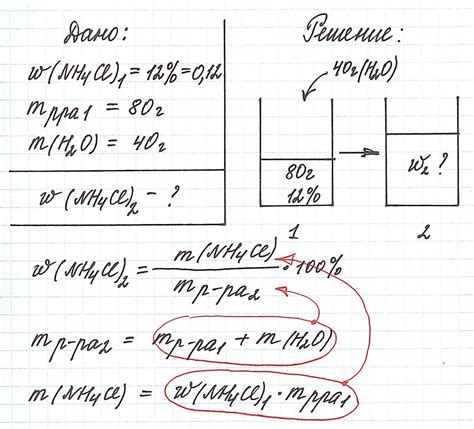
Существует несколько способов выражения концентрации раствора:
1. Массовая концентрация (С) - отношение массы растворенного вещества (m) к объему раствора (V):
C = m/V
2. Объемная концентрация (С) - отношение объема растворенного вещества (V1) к объему раствора (V2):
C = V1/V2
3. Молярная концентрация (С) - отношение количества вещества (n) к объему раствора (V):
C = n/V
Для расчета концентрации раствора необходимо точно измерить массу или объем растворенного вещества с помощью соответствующих инструментов (весы, мерный цилиндр и т.д.). Затем применяются соответствующие формулы для вычисления концентрации раствора, учитывая единицы измерения.
Расчет концентрации раствора является важным шагом в химических расчетах и позволяет определить количество вещества, содержащегося в растворе, а также проводить необходимые дозировки и разведения растворов.
Формула расчета концентрации раствора
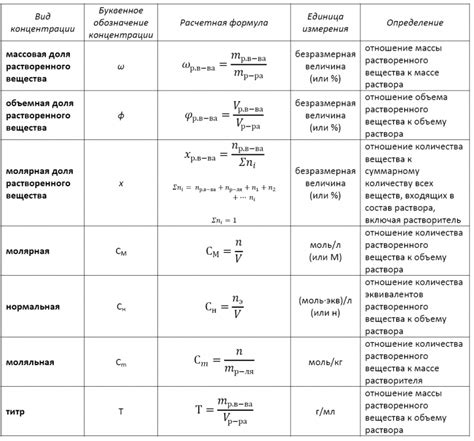
Концентрация (C) = количество растворенного вещества (n) / объем раствора (V)
Формула может быть записана в более компактной форме:
C = n/V
Где:
- C - концентрация раствора;
- n - количество растворенного вещества в молях;
- V - объем раствора в литрах.
При расчете концентрации раствора необходимо учитывать единицы измерения. Если количество растворенного вещества указано в граммах, а объем раствора - в миллилитрах, необходимо преобразовать их в соответствующие единицы измерения.
Например, если количество растворенного вещества указано в граммах, а объем раствора - в миллилитрах, то необходимо преобразовать граммы в моль, используя молярную массу растворенного вещества, и миллилитры в литры, делением на 1000.
Таким образом, формула расчета концентрации раствора играет важную роль в химии, позволяя проводить не только измерения, но и математические расчеты для определения концентрации растворов различных веществ.