Агрегатное состояние – это свойство вещества, определяющее его состояние, то есть физическую форму, в которой оно находится: твердое, жидкое или газообразное. Уникальная способность вещества менять свое агрегатное состояние под воздействием определенных факторов является одной из главных особенностей физических свойств материи.
Агрегатное состояние вещества зависит от нескольких факторов. Во-первых, это температура. Когда температура вещества повышается, его частицы обладают большей энергией движения, что приводит к изменению их взаимного расположения и возникновению новых сил притяжения или отталкивания. Это в свою очередь вызывает изменение агрегатного состояния вещества.
Вторым фактором, влияющим на агрегатное состояние вещества, является давление. Если на вещество действует высокое давление, то частицы начинают сжиматься, и это приводит к уплотнению вещества и переходу его из одного агрегатного состояния в другое. Например, под действием высокого давления газообразное вещество может перейти в жидкое состояние.
Наконец, третьим фактором, определяющим агрегатное состояние вещества, является присутствие примесей. Вещество может находиться в определенном агрегатном состоянии только при условии, что в нем отсутствуют примеси, которые могут изменить его структуру или взаимодействие между частицами. Примеси могут способствовать образованию новых связей между частицами и влиять на их поведение, что может привести к изменению агрегатного состояния вещества.
Что определяет агрегатное состояние вещества?

Агрегатное состояние вещества определяется взаимодействием между его молекулами или атомами. Основные факторы, которые влияют на состояние вещества, включают температуру и давление.
Температура - это мера средней кинетической энергии частиц вещества. Когда температура повышается, кинетическая энергия молекул или атомов растет, что приводит к возрастанию их движения. При достижении определенной температуры, называемой точкой плавления, вещество переходит из твердого в жидкое состояние, а дальнейшее повышение температуры приводит к переходу в газообразное состояние.
Давление также оказывает влияние на агрегатное состояние вещества. При достаточно низком давлении и низкой температуре, межмолекулярные силы удерживают частицы вещества достаточно близко друг к другу, чтобы образовать твердое или жидкое состояние. Однако, при достаточно высоком давлении и/или высокой температуре, молекулы или атомы вещества получают достаточно энергии, чтобы преодолеть эти силы и распространяться в пространстве в виде газа.
Физические свойства вещества

Одним из основных физических свойств вещества является его агрегатное состояние, которое зависит от температуры и давления. В зависимости от этих параметров, вещество может находиться в твёрдом, жидком или газообразном состоянии. Твёрдое состояние характеризуется фиксированной формой и объёмом, а также сильной внутренней связью между частицами. Жидкое состояние обладает переменной формой, но фиксированным объёмом, и меньшей степенью внутренней связи. Газообразное состояние, в свою очередь, испытывает изменение и формы, и объёма, и характеризуется слабыми взаимодействиями между частицами.
Ещё одним важным физическим свойством вещества является его плотность. Плотность определяется отношением массы вещества к его объёму и показывает, насколько вещество концентрировано. Различные вещества имеют разные плотности, что делает это свойство важным при их идентификации и разделении.
Также к физическим свойствам вещества относятся его теплоёмкость, теплопроводность и электропроводность. Теплоёмкость характеризует способность вещества поглощать и отдавать тепло, теплопроводность - способность проводить тепло, а электропроводность - способность проводить электрический ток.
Важно отметить, что физические свойства вещества являются объективными, то есть не зависят от размеров и формы образца, а также от его происхождения. Изучение этих свойств позволяет лучше понять и объяснить поведение вещества в различных условиях и применять их в различных областях науки и техники.
| Физическое свойство | Описание |
|---|---|
| Агрегатное состояние | Определяется температурой и давлением |
| Плотность | Масса вещества, деленная на его объём |
| Теплоёмкость | Способность поглощать и отдавать тепло |
| Теплопроводность | Способность проводить тепло |
| Электропроводность | Способность проводить электрический ток |
Воздействие внешних факторов

При изменении температуры вещество может переходить из одного агрегатного состояния в другое. Например, при нагревании твердого вещества оно может плавиться и перейти в жидкое состояние, а дальнейшее нагревание жидкости приведет к ее испарению и переходу в газообразное состояние. Обратный процесс также возможен - охлаждение газа приведет к его конденсации в жидкость, а затем охлаждение жидкости вызовет ее замерзание в твердое состояние.
Давление также оказывает существенное влияние на состояние вещества. Увеличение давления может вызвать сжатие газа и переход его в жидкое или даже твердое состояние. Напротив, снижение давления может привести к растяжению жидкости и ее испарению в газообразное состояние.
Кроме того, можно выделить и другие факторы, влияющие на агрегатное состояние вещества. Например, наличие растворителя или примешивание других веществ может изменить температуру плавления или кипения вещества. Также влияние оказывает электромагнитное поле, сильные магнитные поля могут вызывать изменение агрегатного состояния вещества.
Молекулярная структура вещества
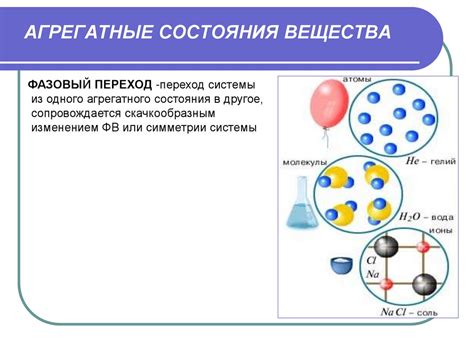
Молекулярные вещества состоят из атомов, которые могут быть одинаковыми или разными. Атомы соединяются между собой с помощью химических связей. В молекулах разных веществ химические связи могут быть разной природы - ковалентными, ионными или металлическими.
Ковалентная связь возникает, когда атомы обменивают электроны, образуя пары электронов. В результате образуется молекула, которая может быть одноатомной или многоатомной. Примером ковалентной связи является водный молекула H2O, состоящая из двух атомов водорода и одного атома кислорода.
Ионная связь возникает между атомами, которые отдают или принимают электроны. В результате образуются положительно и отрицательно заряженные ионы. Примером ионной связи является хлорид натрия (NaCl), состоящий из положительно заряженного иона натрия (Na+) и отрицательно заряженного иона хлора (Cl-).
Металлическая связь возникает между атомами металла, которые делят между собой свои электроны. В результате образуется сеть положительно заряженных ионов металла и свободных электронов. Примером металлической связи является медь (Cu), где положительно заряженные ионы меди образуют сеть, а свободные электроны образуют электронное облако.
Молекулярная структура вещества определяет его физические свойства, такие как температура плавления и кипения, теплоемкость и теплопроводность. Вещества с ковалентными связями обычно имеют низкую температуру плавления и кипения, а вещества с ионными связями - высокую температуру плавления и кипения.
Таким образом, молекулярная структура является ключевым фактором, определяющим агрегатное состояние вещества.