Молярная масса является одним из ключевых понятий в физике и химии. Она позволяет определить массу вещества, содержащегося в одном моле данного вещества. Молярная масса измеряется в г/моль и играет важную роль в различных расчетах и формулах, связанных с химическими реакциями и структурой вещества.
Молярная масса представляет собой отношение массы вещества к количеству вещества в нем. Для расчета молярной массы необходимо знать атомные массы элементов, составляющих данное вещество. Поскольку атомные массы измеряются в атомных единицах массы (аму), они служат основой для расчета молярной массы, которая выражается в граммах на моль.
Молярная масса имеет ряд основных свойств, которые необходимо учитывать при ее использовании. Во-первых, молярная масса указывает на количество граммов вещества, содержащегося в одном моле. Таким образом, она позволяет перейти от количества вещества к его массе и наоборот. Во-вторых, молярная масса позволяет определить состав вещества и выявить, какие элементы присутствуют в нем и в каком количестве.
Определение молярной массы в физике
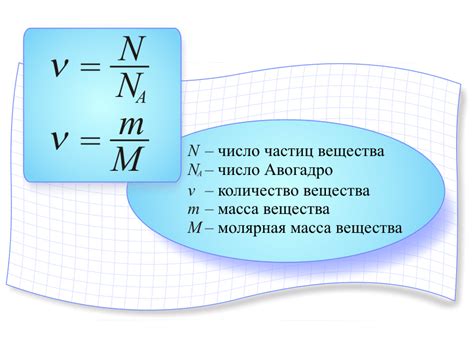
Одним из способов определения молярной массы является соотношение массы вещества к количеству вещества (молям). Для этого необходимо знать массу вещества и его количество по числу молей.
Молярная масса указывается в таблицах химических элементов и соединений. Она позволяет сравнивать разные вещества по их массе и определяет структуру и состав вещества.
Молярная масса является ключевым понятием в химии и физике. Она применяется при расчетах реакций, определении объемов газов и других физических явлений.
Знание молярной массы позволяет более точно определить количество вещества, провести анализ исследуемого материала и применить полученные данные в практических расчетах.
Понятие молярной массы

Молярная масса вычисляется путем сложения атомных масс всех атомов, входящих в состав молекулы вещества. Для этого необходимо знать химическую формулу вещества и массы его атомов, которые указываются в периодической системе элементов.
Например, молярная масса воды (H2O) равна сумме масс двух атомов водорода и одного атома кислорода. Следуя периодической системе элементов, масса одного атома водорода составляет около 1 г/моль, а кислорода - около 16 г/моль. Следовательно, молярная масса воды равна примерно 18 г/моль.
Молярная масса имеет определенные свойства, такие как одинаковая для любого вещества количество вещества в одном моле. Она также позволяет связать относительные массы вещества и количество вещества через коэффициенты в химическом уравнении реакции.
Молярная масса используется в различных расчетах, например, для определения объема газов или концентрации растворов. Она также помогает установить соотношение массы и количества вещества и является важным понятием в химических и физических исследованиях.
Значение молярной массы в химии
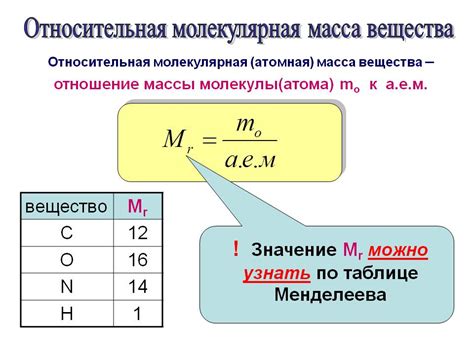
Молярная масса измеряется в граммах на моль (г/моль) и обозначается символом М. Для определения молярной массы вещества необходимо знать его атомную или молекулярную массу.
Молярная масса позволяет связать свойства вещества с количеством вещества в нем. Она позволяет определить количество вещества, выраженное в молях, по известной массе и наоборот.
Пример: для хлора (Cl) атомная масса равна около 35,5 г/моль. Это значит, что в одном моле хлора содержится 35,5 г хлора. Если мы знаем массу хлора, то можем легко определить количество вещества в нем. Например, если у нас есть 71 г хлора, то мы можем сказать, что это 2 моля хлора (2 × 35,5 г).
Значение молярной массы также позволяет расчитать процентное содержание элементов в веществе и определять химические формулы соединений.
Связь между молярной массой и атомной массой

Молярная масса и атомная масса связаны между собой простым математическим соотношением. Молярная масса вычисляется путем сложения атомных масс всех атомов в молекуле вещества. Таким образом, молярная масса может быть рассчитана как сумма атомных масс, деленная на количество атомов в молекуле.
Формула для вычисления молярной массы выглядит следующим образом:
Молярная масса = (Атомная масса1 × Количество атомов1) + (Атомная масса2 × Количество атомов2) + ...
Например, для молекулы воды (H2O) молярная масса может быть вычислена следующим образом:
Молярная масса воды = (Атомная масса водорода × 2) + Атомная масса кислорода = (1 г/моль × 2) + 16 г/моль = 18 г/моль
Таким образом, молярная масса воды равна 18 г/моль.
Зная молярную массу вещества, мы можем определить количество вещества (в молях) по известной массе. Для этого нужно разделить массу вещества на его молярную массу. Например, если имеется 36 г воды, можно рассчитать количество молей следующим образом:
Количество молей = Масса вещества / Молярная масса = 36 г / 18 г/моль = 2 моль
Таким образом, имеется 2 моля воды.
Связь между молярной массой и атомной массой позволяет установить количественные соотношения между массой вещества и его составляющими атомами. Это основное свойство молярной массы, которое позволяет проводить различные расчеты, связанные с количеством вещества и его составом.
Методы определения молярной массы
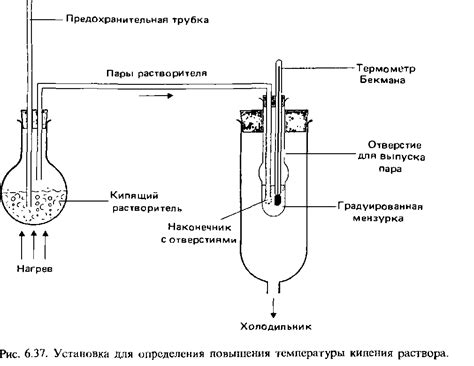
1. Методы газовых изотопов: Этот метод основан на измерении отношений масс молекул вещества с разными изотопами. Путем измерения диффузии или использования масс-спектрометрии можно определить отношение масс двух изотопов и вычислить молярную массу.
2. Методы осмотического давления: Осмотическое давление зависит от молярной массы растворенного вещества. Измерение осмотического давления позволяет определить молярную массу путем сравнения с давлением идеального раствора.
3. Методы криоскопии и теплоты растворения: Криоскопия основана на изменении точки замерзания раствора при добавлении растворенного вещества. Теплота растворения используется для вычисления молярной массы путем известных констант и изменения температуры растворения.
4. Методы определения плотности: Плотность вещества связана с его молярной массой. Определение плотности и использование известных формул позволяет вычислить молярную массу.
5. Методы хроматографии: Хроматографические методы позволяют разделить смесь веществ по их аффинности и учитывать их массу для определения молярной массы.
Определение молярной массы вещества является важным шагом в понимании его свойств и способностей взаимодействия с другими веществами. Различные методы определения молярной массы обеспечивают возможность получить точные и достоверные значения этой характеристики.
Роль молярной массы в расчетах

Одним из основных применений молярной массы является расчет количества вещества в образце. Зная молярную массу и массу образца, можно определить число молей вещества по формуле:
число молей = масса образца / молярная масса
Это отношение позволяет определить, сколько вещества содержится в данном образце и сравнивать количество вещества в различных образцах.
Кроме того, молярная масса позволяет проводить расчеты, связанные с реакцией между разными веществами. Зная молярные массы реагентов и их соотношение в уравнении реакции, можно определить массу продукта или массу реагента, участвующего в реакции.
Также, молярная масса может быть использована для определения плотности газов. Зная молярную массу газа и его плотность при нормальных условиях, можно определить плотность газа при любых других условиях.
Таким образом, молярная масса играет важную роль в физических расчетах и позволяет проводить различные анализы и эксперименты, связанные с составом и свойствами вещества.
Важность молярной массы в физических экспериментах

Одно из применений молярной массы заключается в определении количества вещества. Молярная масса позволяет перевести массу вещества из граммов в моль. Это особенно полезно при проведении химических экспериментов, где точное определение количества вещества является важным шагом для правильного проведения реакций.
Кроме того, молярная масса позволяет проводить сравнительные исследования различных веществ. Используя молярные массы, можно производить сравнение плотностей разных материалов, исследовать их физические свойства, определять распределение энергии вещества, рассчитывать количество вещества, необходимое для достижения определенных результатов.
Также молярная масса используется для определения структуры и состава молекул. Зная молярную массу, можно производить расчеты, связанные с электронной структурой вещества, определением молекулярного размера и формы молекулы. Это помогает понять, как взаимодействуют молекулы вещества и какие физические и химические свойства они проявляют.
Таким образом, молярная масса играет важную роль в физических экспериментах, позволяя исследователям проводить точные расчеты и сравнивать различные вещества. Ее значение простирается не только на химические исследования, но также на физические исследования в различных отраслях науки. Понимание и использование молярной массы является основой для дальнейших расчетов и анализа результатов экспериментов.