Аммиак – это одно из наиболее распространенных химических соединений, используемых в промышленности и быту. Он широко применяется в качестве удобрения для сельскохозяйственных культур, а также в производстве химических и фармацевтических продуктов. Но что происходит, когда аммиак растворяется в воде? Ответ на этот вопрос представляет научный интерес и имеет практическое значение.
Растворение аммиака в воде приводит к возникновению раствора, который известен под названием аммиачной воды. Образование этого раствора происходит благодаря процессу обратимой химической реакции, которая позволяет аммиаку растворяться в воде в определенном соотношении.
В растворенном состоянии аммиак образует аммонийные ионны, которые являются основанием амфотерного характера. Это означает, что аммиак может действовать как кислота или основание, в зависимости от окружающей среды. При растворении в воде, аммиак выступает в качестве основания и образует аммонийные ионы и гидроксидные ионы, характерные для щелочной среды.
Что происходит при растворении аммиака в воде
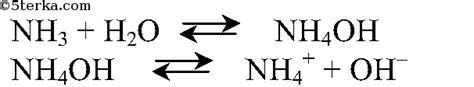
Аммиак (NH3) может быть растворен в воде, образуя аммиачный раствор. Этот процесс характеризуется рядом особенностей и имеет важные применения в различных областях науки и промышленности.
При растворении аммиака в воде происходит образование ионов аммония (NH4+) и гидроксид-ионов (OH-). Ионный характер аммиачного раствора приводит к образованию щелочной среды, так как гидроксид-ионы, являясь слабыми основаниями, обеспечивают алкалическую реакцию водного раствора.
| Основные свойства аммиачного раствора: |
|---|
| 1. Повышенная щелочность. |
| 2. Неприятный запах. |
| 3. Хорошая растворимость в воде. |
| 4. Эндотермическая реакция при растворении. |
В промышленности аммиачный раствор используется в различных процессах, таких как пищевая промышленность, фармацевтика, производство удобрений и многие другие. Кроме того, аммиачный раствор играет важную роль в химическом анализе и медицине.
Химическая реакция аммиака с водой

Когда аммиак растворяется в воде, происходит химическая реакция, называемая гидратацией. Реакция представляет собой образование гидроксида аммония (NH4OH). Во время гидратации аммиака связь N-H разрывается, а атом водорода (H) переходит на кислородный атом (O) воды, образуя молекулу гидроксида аммония.
Таким образом, реакция аммиака с водой может быть представлена следующим уравнением:
NH3 + H2O → NH4OH
Образовавшийся гидроксид аммония (NH4OH) является слабой щелочью, которая умеренно ионизируется в растворе, образуя аммонийные и гидроксидные ионы:
NH4OH → NH4+ + OH-
Гидроксидные ионы (OH-) придают раствору щелочные свойства и способствуют его щелочной реакции. Аммонийные ионы (NH4+) также могут образовывать аммонийные соли с различными кислотами.
Физические свойства растворов аммиака

Первой важной характеристикой растворов аммиака является их аммиаковая концентрация. Растворы аммиака могут иметь различную концентрацию, которая измеряется в процентах. Наиболее распространены растворы аммиака с концентрацией от 10% до 30%. Эти растворы обычно используются в бытовых условиях, например, для очистки и дезинфекции поверхностей.
Вторым важным физическим свойством растворов аммиака является их pH-значение. Растворы аммиака являются основными, то есть имеют pH выше 7. Чем выше концентрация аммиака в растворе, тем выше его pH-значение. Это делает их эффективными в качестве очищающих средств и средств для регулирования pH-уровня в различных процессах.
Третьим важным физическим свойством растворов аммиака является их температура кипения. Растворы аммиака кипят при нижних температурах по сравнению с пустой водой. Например, при растворении аммиака с концентрацией 25% вода может начать кипеть уже при температуре около 37 градусов по Цельсию. Такие свойства растворов аммиака позволяют использовать их в низкотемпературных процессах и системах охлаждения.
Таким образом, растворы аммиака обладают определенными физическими свойствами, которые определяют их широкое применение в различных областях. Они отличаются аммиаковой концентрацией, pH-значением и температурой кипения, что позволяет использовать их в различных процессах и приложениях.
Влияние растворенного аммиака на окружающую среду

Растворенный аммиак имеет отличное влияние на окружающую среду. Первоначально, молекулы аммиака могут быть выпущены в атмосферу и образовать осадки. Затем, при контакте с водой, аммиак может раствориться в резервуарах и открытых водоемах, таких как озера и реки. Это может привести к увеличению уровня аммиака в воде и негативно влиять на местные экосистемы.
Высокая концентрация аммиака в растворе может иметь токсические последствия. Он может оказывать вредное воздействие на рыб и других водных организмов, например, вызывая у них задыхание или повреждение жабр. Повышенная концентрация аммиака может также приводить к изменению pH воды, что может повлиять на рост и размножение водных организмов и других экологических систем.
Однако, следует отметить, что аммиак имеет множество полезных применений в промышленности, сельском хозяйстве, бытовых товарах и медицине. Он может быть использован как удобрение для сельскохозяйственных культур и как ингредиент в производстве пищевых продуктов. Однако, для минимизации негативного влияния на окружающую среду необходимо контролировать его использование и выпуск в окружающую среду.
Биологическое действие аммиака в растворе

Биологическое действие аммиака в растворе обусловлено его способностью раздражать слизистые оболочки, кожу и глаза. Если аммиакный раствор попадает на кожу, он может вызвать ожоги, покраснение и опухание. Контакт с глазами может вызвать серьезные повреждения роговицы и даже потерю зрения.
Кроме того, аммиакный раствор является сильным раздражителем дыхательных путей. При его вдыхании возникают ощущение дискомфорта, кашель, затрудненное дыхание и раздражение слизистых оболочек. Длительное воздействие аммиака на организм может привести к более серьезным последствиям, таким как развитие астмы или хронического бронхита.
В случае попадания аммиака в организм через устную полость, он может вызвать ожоги слизистой оболочки рта, гортани и пищевода. При проглатывании больших доз аммиака возможно отравление, сопровождающееся тошнотой, рвотой, болями в желудке и нарушением общего состояния.
Необходимо помнить, что аммиакный раствор обладает высокой токсичностью и может представлять опасность для живых организмов, включая растения и животных. Он может повредить или уничтожить клетки, нарушить функции органов и вызвать различные патологические изменения.
В связи с этим, при работе с аммиаком и его растворами необходимо соблюдать меры предосторожности, включая использование защитной одежды, масок, очков и перчаток. В случае попадания аммиака на кожу или в глаза, следует незамедлительно промыть их большим количеством воды и обратиться за медицинской помощью.
Применение растворов аммиака в различных отраслях
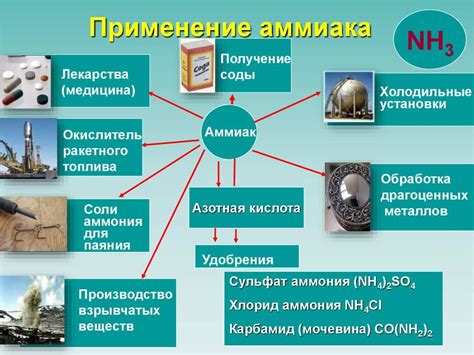
Один из основных и наиболее распространенных способов применения аммиака - это его растворение в воде. Растворы аммиака получают путем смешивания определенного количества аммиака и воды в заданных пропорциях. Такие растворы обладают рядом уникальных свойств и находят широкое применение в различных отраслях.
Одно из основных направлений применения растворов аммиака - это производство удобрений. Растворы аммиака являются ценным источником азота для растений, необходимого для их роста и развития. Аммиак может быть использован в качестве удобрения самостоятельно, или в составе комплексных удобрений.
Кроме того, растворы аммиака нашли широкое применение в химической, фармацевтической и пищевой промышленности. Они используются в процессах синтеза различных органических соединений, производстве лекарственных препаратов и добавок к пище. Растворы аммиака также широко применяются в химическом анализе и лабораторной практике.
Благодаря своим антимикробным свойствам, растворы аммиака использовались в прошлом для дезинфекции лечебных помещений и инструментов. В настоящее время, с развитием более эффективных и безопасных методов, применение аммиака в этой области сократилось, но его растворы все еще находят применение в сельском хозяйстве для дезинфекции животных помещений и принадлежностей.
| Отрасль | Применение растворов аммиака |
|---|---|
| Производство удобрений | Источник азота для растений |
| Химическая промышленность | Синтез органических соединений |
| Фармацевтическая промышленность | Производство лекарственных препаратов |
| Пищевая промышленность | Добавки к пище |
| Анализ и лабораторная практика | Химический анализ и качественный анализ |
| Сельское хозяйство | Дезинфекция животных помещений и принадлежностей |
Растворы аммиака имеют множество других применений, и их значимость в различных отраслях несомненна. Однако, при работе с растворами аммиака необходимо соблюдать осторожность и соблюдать меры безопасности, так как аммиак является токсичным веществом.
Особенности использования растворов аммиака

Первое и наиболее важное свойство растворов аммиака – это их щелочной характер. При растворении аммиака в воде он образует аммонийные и гидроксидные ионы. Именно поэтому растворы аммиака обладают щелочными свойствами и обычно имеют pH значительно выше 7. Их способность нейтрализовать кислоты, образуя соли, делает растворы аммиака ценными для использования в различных химических процессах и промышленности.
Второе важное свойство растворов аммиака – это их способность образовывать аммиаковые соли. Благодаря высокой растворимости аммиаковых солей, растворы аммиака широко применяются в сельском хозяйстве как удобрения. Аммонийные соли, такие как сульфат аммония или нитрат аммония, содержат азот, который является необходимым элементом для роста растений. Растворы аммиака способствуют улучшению плодородия почвы и повышению урожайности растений.
Третье важное свойство растворов аммиака – это их способность обладать хлоросодержащими свойствами. Аммиаковые растворы, содержащие дополнительно хлор, называют аммиаком-хлоридом. Такие растворы нашли широкое применение в медицине и фармацевтике, а также в процессе производства бумаги, кожи и текстиля.
Кроме того, растворы аммиака имеют характерный запах, который обусловлен высокой летучестью аммиака. Это может быть полезно при обнаружении утечек или при использовании в процессе очистки воздуха от вредных газов.
В целом, растворы аммиака представляют собой важный химический продукт, обладающий различными полезными свойствами и широким спектром применения в различных отраслях промышленности и сельского хозяйства.