Изоэлектрическая точка – это значение рН, при котором белок в среде обладает нейтральным электрическим зарядом. Но что происходит с белком, когда оно находится в этой точке?
Изоэлектрическая точка является ключевым показателем для многих биохимических исследований, поскольку она может влиять на свойства и функции белков. Например, при изоэлектрическом фокусировании, методе разделения белков по их заряду, используется их различие в пКа значениях аминокислотных остатков и изоэлектрических точках.
Когда белок находится в своей изоэлектрической точке, его поверхностные заряды полностью компенсируются, что приводит к сокращению сил притяжения и отталкивания между молекулами белка. Это может влиять на растворимость белка и образование агрегатов. Кроме того, свойства белков, такие как их активность, стабильность и взаимодействие с другими молекулами, также могут изменяться в зависимости от их изоэлектрической точки.
Изоэлектрическая точка и её определение
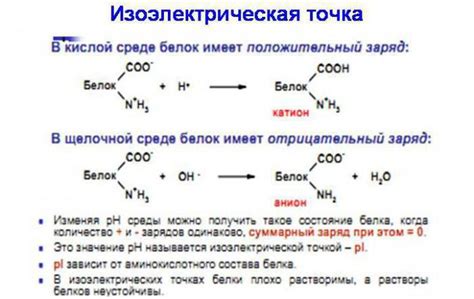
Определение изоэлектрической точки требует знания аминокислотного состава белка и pK-значений его функциональных групп. Для наиболее точной оценки pI используются различные методы, включая изоэлектрическую фокусировку (isoelectric focusing) и электрофорез в градиентном геле (gel electrophoresis).
Знание изоэлектрической точки белка является важным для его изучения и эксплуатации. Оно позволяет определить заряд белка в зависимости от окружающей среды, что влияет на его структуру и функцию. Также изоэлектрическая точка является ключевым параметром при проведении методов, основанных на фокусировке и разделении белков, таких как изоэлектрическая фокусировка и хроматография на ионитах.
Понятие и значение
Знание и понимание значения изоэлектрической точки важно для многих процессов, связанных с белками. Например, при очистке и концентрировании белков используется метод изоэлектрической фокусировки, основанный на разделении белков по их заряду. Этот метод позволяет эффективно разделить и очистить белки с разными pI.
Важным аспектом изоэлектрической точки является ее связь с аминокислотным составом белка. Разные аминокислоты имеют разные pKa (константу диссоциации кислоты), что влияет на их заряд в зависимости от pH. Поскольку белки состоят из аминокислотных остатков, их изоэлектрическая точка определяется суммарным вкладом аминокислот в их аминокислотный состав.
Значение изоэлектрической точки и связанные с ней реакции белков имеют важное значение в биохимии, фармакологии, медицине и других областях науки, где изучаются белки и их функции.
| Название | Определение |
|---|---|
| pH | Мера кислотности или щелочности водных растворов, указывающая на концентрацию ионов водорода (H+). |
| Молекула белка | Молекула, состоящая из аминокислотных остатков, служащая строительным материалом и выполняющая различные функции в организме. |
| Цепь белка | Связанные последовательно аминокислотные остатки, составляющие молекулу белка и определяющие его структуру и функцию. |
| Коагулирование | Процесс свертывания белковой цепи в плотную структуру, вызванного изменением pH или другими факторами. |
| pI (изоэлектрическая точка) | Значение pH, при котором белок не несет электрический заряд и находится в нейтральном состоянии. |
| Изоэлектрическая фокусировка | Метод разделения белков на основе различия их заряда при определенном pH, используется в белковых характеризации и очистке. |
| pKa (константа диссоциации кислоты) | Константа, определяющая кислотные свойства аминокислотных остатков. |
Физическое значение
Изоэлектрическая точка является важным критерием при изоляции, очистке и дроблении белкового сырья. В зоне изоэлектрической точки молекулы белка могут быть прошарки, связанные с высокой гидрофобностью или гидрофильностью среды, что позволяет эффективно применять методы сепарации. Кроме того, заряд белка при изоэлектрической точке влияет на его связывание с лигандами, реакцию ферментов и другие биохимические процессы.
Экспериментальное определение изоэлектрической точки основано на изменении заряда белка с изменением pH среды. Для этого используют различные методы, такие как изоэлектрофокусировка и изоэлектрическая экстракция. Определение изоэлектрической точки позволяет улучшить методы анализа белков и получение чистых препаратов для исследований и промышленности.
Влияние изоэлектрической точки на белок

Изоэлектрическая точка (pHiso) представляет собой значение рН, при котором электрический заряд белка равен нулю. При данном значении рН молекула белка не имеет электрического заряда и, следовательно, не притягивается ни к положительно, ни к отрицательно заряженным частицам.
Эффект изоэлектрической точки на белок важен для его физико-химических свойств и функций в организме. Наиболее заметное влияние наблюдается на структуру и растворимость белка.
Важное свойство изоэлектрической точки заключается в возможности использования ее значения для электрофракционирования белков. Путем установления определенного значении рН можно разделить смеси белков на отдельные компоненты, исходя из их различий в изоэлектрических точках.
Изменение значения рН может привести к изменению структуры белка и его активности. Например, изменение изоэлектрической точки может вызвать изменение конформации белка и влиять на его способность связываться с другими молекулами или биологическими структурами.
Кроме того, значение изоэлектрической точки можно использовать для определения пищевой ценности и качества белковых продуктов. Значение изоэлектрической точки может указывать на стабильность и изменения в структуре белка, что может быть важно для производства пищевых продуктов.
Таким образом, изоэлектрическая точка играет существенную роль в физико-химических свойствах и функциях белка. Значение этой точки имеет важное значение для его структуры, функциональности и потенциальных приложений в различных областях, включая биотехнологию и пищевую промышленность.
Аминокислоты и их заряды
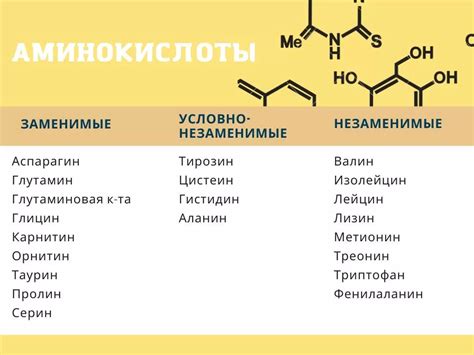
Каждая аминокислота имеет различные свойства, включая свою химическую структуру и заряд. Заряд аминокислоты зависит от рН окружающей среды.
В позитивно заряженных аминокислотах, таких как аргинин, лизин и гистидин, аминогруппа имеет положительный заряд. Они способны принимать дополнительные протоны и имеют большую склонность к образованию солей с отрицательно заряженными группами.
В отрицательно заряженных аминокислотах, таких как аспартат и глютамат, боковая цепь имеет отрицательный заряд. Они способны отдавать протоны и также могут образовывать соли с положительно заряженными группами.
В аминокислотах нейтрального заряда, таких как аланин, глицин и валин, аминогруппа и боковая цепь не имеют заряда и не могут образовывать ионы.
Изменение заряда аминокислоты может влиять на ее взаимодействие с другими молекулами и реактивностью. Например, изменение пН окружающей среды может привести к изменению заряда аминокислоты и, следовательно, к изменению свойств белка в целом.
Изоэлектрическая точка (pI) – это тот pН, при котором аминокислота имеет нулевой заряд. Изоэлектрическая точка белка – это тот pН, при котором нет электрической разности между его частями, что обеспечивает ему наиболее стабильную структуру.
Изоэлектрическая точка может быть использована для разделения и очистки различных белковых фракций, так как белки имеют различные заряды при разных значениях pН. Изоэлектрическая фокусировка – это метод разделения белков, основанный на их заряде в зависимости от pН окружающей среды.
Роль pH-значения в изменении заряда белка
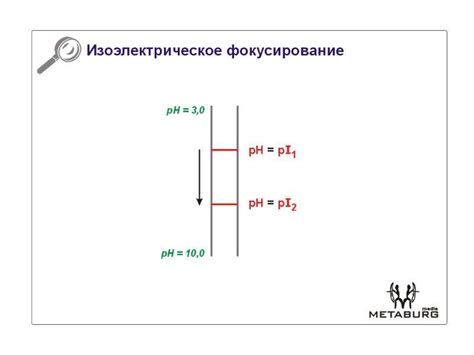
Когда pH-среды равно изоэлектрической точке (pI), заряд белка равен нулю. Изоэлектрическая точка - это та точка pH, при которой молекула белка не имеет никакого чистого электрического заряда. В этом состоянии белок наиболее устойчив и имеет минимальное взаимодействие с другими молекулами.
Когда pH-значение окружающей среды отличается от pI, заряд белка становится отрицательным или положительным. Это происходит из-за наличия кислотных или щелочных групп на белке, которые могут принимать или отдавать протоны в зависимости от pH. Кислотные группы, такие как карбоксильные, отдают протоны при повышении pH, тем самым делая белок отрицательно заряженным. Наоборот, щелочные группы, такие как аминогруппы, принимают протоны при понижении pH, делая белок положительно заряженным.
Изменения заряда белка в зависимости от pH-значения играют важную роль в его структуре и функции. Во-первых, заряд белка может влиять на его связывание с другими молекулами, такими как ферменты или антигены. Заряд белка также может влиять на его растворимость в воде и его способность переноситься через мембраны.
| pH среды | Заряд белка |
|---|---|
| Меньше pI | Положительный |
| Больше pI | Отрицательный |
| Равно pI | Нулевой |
Проявление изоэлектрической точки в практической биологии

Проявление изоэлектрической точки в практической биологии имеет несколько важных аспектов:
1. Использование изоэлектрической фокусировки: Изоэлектрическая фокусировка является одним из методов разделения и чистки белков. Она основана на использовании различия в заряде белков при разных значениях pH. Путем поддержания постоянного pH в градиенте ионитов, белки мигрируют к точке изоэлектрического фокусирования, где останавливаются из-за отсутствия заряда и образуют острую зону. Этот метод позволяет разделить исходную смесь белков на компоненты с разными изоформами и эффективно очистить их.
2. Определение положения изоэлектрической точки: Знание pI белка является важным с точки зрения его растворимости и стабильности. Белки с низким pI имеют разительное поведение в различных условиях pH и могут быть менее стабильными или плохо растворимыми при негативных или экстремальных значениях pH. Определение pI белка может помочь в выборе оптимальных условий хранения и обработки.
3. Влияние изоэлектрической точки на взаимодействие белков: Заряд белка, определяемый его pI, играет важную роль в его взаимодействии с другими молекулами. Например, заряженные аминокислоты на поверхности белка могут привлекать или отталкивать другие белки или лиганды. Понимание изоэлектрической точки белка может помочь предсказать его взаимодействие с другими молекулами и способствовать разработке новых терапевтических препаратов и диагностических методов.
Таким образом, изоэлектрическая точка имеет важное значение в практической биологии, позволяя разделять белки, определять их стабильность и растворимость, а также предсказывать их взаимодействие с другими молекулами.
Изоэлектрическая фокусировка
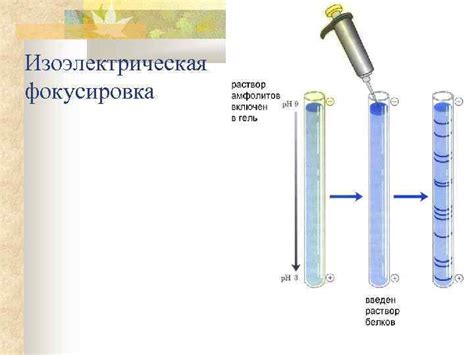
Процедура изоэлектрической фокусировки проводится в специальной электрофоретической камере, в которую помещается градиентная гель-колонка. Градиентная гель-колонка состоит из геля с изменяющимся pH-значением от одного края к другому. Когда смесь белков наносится на колонку, они вступают в контакт с гелевой матрицей и начинают перемещаться в направлении своей изоэлектрической точки.
Во время процесса белки полностью останавливаются на том участке геля, где pH равен их pI, так как их заряд становится равным нулю. Это называется фокусировкой, и в этот момент каждый белок фиксируется на геле.
После завершения процедуры осуществляется извлечение белков из геля для дальнейшего анализа. Это можно сделать путем разъединения геля или искусственного изменения условий, в результате которых белки приобретут заряд и снова начнут двигаться.
Изоэлектрическая фокусировка является важным методом разделения белков в биохимических исследованиях. Ее применяют для изучения структуры и свойств белков, а также для анализа иллирования, модификации и секвенирования белков.
| Преимущества изоэлектрической фокусировки: | Недостатки изоэлектрической фокусировки: |
|---|---|
| Позволяет разделять белки на основе их изоэлектрической точки без воздействия на их структуру. | Требует специализированного оборудования и материалов. |
| Очень высокая разделяющая способность и чувствительность. | Долгий процесс разделения белков. |
| Может использоваться для анализа больших смесей белков. | Требует аккуратной подготовки и манипуляций с гелями и белками. |