Сродство к электрону - это важное понятие в атомной физике, которое описывает способность атомов привлекать и удерживать электроны. Интересно, что сродство к электрону может меняться в зависимости от различных факторов, таких как химический элемент, окружающая среда и внешние условия.
Сродство к электрону является фундаментальным свойством атома, влияющим на его химические и физические свойства. Высокое сродство к электрону означает, что атом легко привлекает электроны и образует с ними стабильные химические связи. Напротив, низкое сродство к электрону указывает на то, что атом не обладает большой способностью привлекать электроны и может легко отдавать их другим атомам.
Сродство к электрону может изменяться в зависимости от положения элемента в периодической системе. Например, сродство к электрону увеличивается к основанию группы в периодической системе, что обусловлено увеличением размера атомов и уменьшением эффективности экранирования электронных оболочек. Также сродство к электрону может изменяться в зависимости от окружающей среды и наличия других атомов или молекул рядом с атомом.
Понятие сродства к электрону

Сродство к электрону обычно измеряется в электрон-вольтах (эВ) или килоджоулях на моль (кДж/моль). Чем больше значение сродства к электрону у атома, тем сильнее его притяжение к электрону и тем больше энергии требуется для отделения электрона от атома.
Сродство к электрону может меняться в зависимости от различных факторов, таких как химический элемент, его электронная конфигурация и окружающая среда. Например, атомы из группы алкалинных металлов имеют низкое сродство к электрону, что делает их хорошими донорами электронов, в то время как атомы галогенов имеют высокое сродство к электрону и могут легко принять дополнительные электроны.
Сродство к электрону также может быть связано с атомным радиусом. Чем меньше атомный радиус, тем ближе электроны находятся к ядру, и тем сильнее их притяжение. Поэтому атомы с малым атомным радиусом имеют обычно большее сродство к электрону.
Знание сродства к электрону позволяет предсказывать и объяснять химические свойства элементов и их реакционную способность. Это знание является основой для понимания молекулярной и атомной химии и находит применение в различных отраслях науки и промышленности.
Определение и основные принципы
Основные принципы сродства к электрону:
| Принцип | Описание |
|---|---|
| Принцип максимального сродства | Атом стремится образовать связи таким образом, чтобы его энергия была минимальной. Для этого он может принимать, отдавать или делить электроны с другими атомами. |
| Принцип электронной оккупации | При формировании химических соединений атомы заполняют свои энергетические уровни по принципу минимальной энергии, начиная с нижних уровней. |
| Принцип оптимального распределения зарядов | Атомы стремятся к образованию структур со сбалансированным распределением зарядов, чтобы минимизировать кулоновское отталкивание. |
Сродство к электрону является важным понятием в химии, так как оно позволяет понять, каким образом происходят реакции образования химических соединений и почему некоторые соединения стабильны, а другие нет.
Важность сродства к электрону
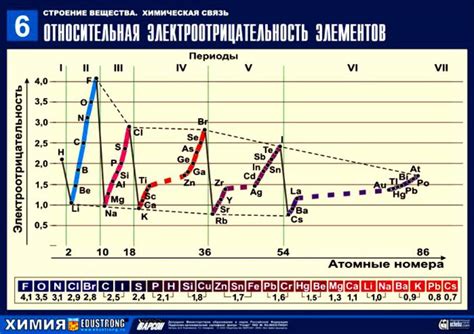
Сродство к электрону имеет огромное значение в контексте химических реакций и физических свойств веществ. Знание и понимание сродства к электрону позволяет предсказывать и объяснять множество феноменов и явлений, происходящих на молекулярном и атомарном уровне.
Благодаря сродству к электрону мы можем объяснить, почему некоторые вещества обладают высокой активностью в реакциях, тогда как другие вещества проявляют пассивность. Сродство к электрону определяет, насколько сильно элемент или молекула притягивает электроны к себе. Это важный индикатор реакционной способности вещества и его химической активности.
Сродство к электрону также определяет свойства различных соединений и их способность к образованию связей. Например, элементы с высоким сродством к электрону легко образуют отрицательные ионы, так как готовы принять дополнительные электроны. С другой стороны, элементы с низким сродством к электрону предпочитают отдавать электроны и образовывать положительные ионы.
Знание сродства к электрону помогает разобраться в свойствах веществ, таких как проводимость электричества, теплопроводность, реакционная способность и даже цвет. Сродство к электрону играет ключевую роль в понимании химических и физических процессов, а также находит широкое применение в различных областях, начиная от химии и физики и заканчивая биологией и материаловедением.
Факторы, влияющие на сродство
1. Заряд ядра атома. Чем больше заряд ядра, тем больше сродство. Ведь сильное ядро притягивает электроны сильнее и удерживает их ближе к себе.
2. Расстояние от электрона до ядра. Чем ближе электрон к ядру, тем сильнее силы притяжения между ними, и, следовательно, сродство будет выше.
3. Электронная конфигурация атома. Сродство может меняться в зависимости от расположения электронов в энергетических уровнях атома. Например, атомы с полностью заполненными энергетическими уровнями обладают высоким сродством, так как электроны труднее удалить из стабильной конфигурации.
4. Валентность атома. Атомы с полной внешней оболочкой электронов (например, инертные газы) обладают высоким сродством, так как они стремятся сохранить стабильность своей электронной конфигурации.
5. Электроотрицательность атома. Чем больше электроотрицательность атома, тем больше его сродство. Атомы с большой электроотрицательностью сильнее притягивают электроны к себе, поэтому сродство будет выше.
Различные факторы оказывают влияние на сродство к электрону. Изучение этих факторов позволяет лучше понять структуру и свойства атомов и элементов, что имеет большое значение в области химии и материаловедения.
Изменение сродства в разных условиях

Одним из факторов, влияющих на сродство к электрону, является окружающая среда. Когда атом находится в агрессивной среде, с малым количеством электронов, его сродство к электрону будет высоким. В таких условиях атом стремится привлечь дополнительный электрон для стабилизации своей электронной конфигурации.
С другой стороны, в среде, насыщенной электронами, сродство к электрону будет низким. В таких условиях атом уже имеет достаточное количество электронов и не нуждается в привлечении дополнительных.
Также, сродство к электрону может зависеть от температуры. При повышении температуры в системе, сродство к электрону может изменяться. Это связано с тем, что при высоких температурах энергия частиц увеличивается, что может сказываться на вероятности их взаимодействия с электроном.
Изменение сродства к электрону в зависимости от различных условий является важным фактором во многих процессах и явлениях в химии и физике. Понимание этих изменений помогает уточнить модели и теории, описывающие взаимодействие атомов и электронов в различных системах.
Сродство к электрону в химических реакциях

Сродство к электрону может меняться в зависимости от различных факторов, включая химический элемент, окружающую среду и структуру молекулы. Обычно сродство к электрону увеличивается по периодической таблице с уменьшением номера группы элементов. Это связано с увеличением энергетического уровня, на котором находится последняя заполняемая оболочка электронов.
В химических реакциях атомы и молекулы могут принимать или отдавать электроны, чтобы достичь стабильной электронной конфигурации. Атомы, имеющие низкое сродство к электрону, имеют тенденцию отдавать электроны, образуя положительно заряженные ионы. Атомы с высоким сродством к электрону, наоборот, имеют тенденцию принимать электроны, образуя отрицательно заряженные ионы.
Сродство к электрону играет ключевую роль в множестве химических процессов, включая реакции окисления-восстановления, образование химических связей и катализ. Химические реакции могут изменять сродство к электрону атомов и молекул, что приводит к образованию новых соединений и обмену электронами.
Для более детального изучения сродства к электрону в химических реакциях применяются различные методы, такие как электронно-структурный анализ и квантово-химические расчёты. Эти методы позволяют определить энергию, связанную с присоединением или отделением электрона, а также исследовать электронные конфигурации и строение молекул.
| Элемент | Сродство к электрону (эВ) |
|---|---|
| Литий (Li) | 0,618 |
| Кислород (O) | 1,461 |
| Фтор (F) | 3,399 |
Применение сродства к электрону
Одним из основных применений сродства к электрону является химическая реакционная способность веществ. Вещества с большим сродством к электрону легче принимают или отдают электроны, что способствует их взаимодействию с другими веществами и участию в различных химических реакциях.
Также, сродство к электрону находит применение в электронике и полупроводниковой технике. Материалы с высоким сродством к электрону используются в создании полупроводниковых компонентов, таких как диоды и транзисторы. Благодаря своей способности притягивать электроны, эти материалы позволяют контролировать ток электронов и создавать различные электронные устройства.
Сродство к электрону также играет важную роль в каталитических процессах. Катализаторы с высоким сродством к электрону способны ускорять химические реакции, участвуя в промежуточных этапах реакций и облегчая прохождение электронов между реагентами.
Сродство к электрону также имеет значительное значение в биологических системах. Оно определяет взаимодействие атомов и молекул в биохимических реакциях, таких как окислительно-восстановительные процессы. Благодаря сродству к электрону различных молекул, биологические системы обеспечивают жизненно важные процессы, такие как дыхание и обмен веществ.