Масса и количество молекул вещества являются основными понятиями в химии, и изучение их взаимосвязи позволяет понять множество физико-химических процессов. Азот (N) - это весьма распространенный элемент в природе, входящий в состав многих органических и неорганических соединений. Измерить его массу можно различными способами, и одним из интересных вопросов является определение массы определенного количества молекул азота.
Для ответа на вопрос о массе 10^22 молекул азота необходимо знать молярную массу данного элемента. Молярная масса азота равна примерно 14 г/моль. Это означает, что масса одного моля атомов азота составляет 14 г. При этом, одна моль вещества содержит 6.02*10^23 молекул. Таким образом, масса одной молекулы азота составляет примерно 2.32*10^-23 г.
Теперь, зная массу одной молекулы азота, можно определить массу 10^22 молекул данного элемента. Для этого необходимо умножить массу одной молекулы на количество молекул:
Масса = (2.32*10^-23 г/молекула) * (10^22 молекул) = 2.32 г
Таким образом, масса 10^22 молекул азота равна примерно 2.32 г. Имея данные о молярной массе и количестве молекул, можно рассчитывать массу любого количества азота и проводить дальнейшие расчеты в химических реакциях и прочих процессах.
Масса 10^22 молекул азота
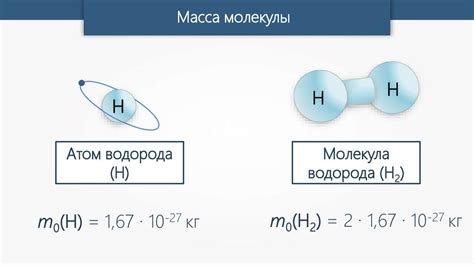
Масса молекулы азота (N2) составляет примерно 28 атомных единиц массы, а молярная масса азота (N) равна 14 атомным единицам массы (г/моль).
Чтобы вычислить массу 10^22 молекул азота, нужно умножить молярную массу азота (14 г/моль) на количество молекул.
- 1 моль N2 молекул содержит примерно 6.022 x 10^23 молекул
- 10^22 молекул N2 = (10^22 молекул / 6.022 x 10^23 молекул/моль) моль N2
Подставив числа в формулу, получим:
Масса 10^22 молекул азота = (14 г/моль) * (10^22 молекул / 6.022 x 10^23 молекул/моль) = 2.322 г
Таким образом, масса 10^22 молекул азота составляет примерно 2.322 г.
Свойства азота

Азот - безцветный, безвкусный и неприятно пахнущий газ при нормальных условиях. Он не реагирует с кислородом, водой и некоторыми кислотами, поэтому широко применяется в сельском хозяйстве в качестве удобрения для повышения плодородия почвы.
Физические свойства азота:
- Температура плавления: -210 °C
- Температура кипения: -196 °C
- Плотность: 1,25 г/л
- Молярная масса: 28 г/моль
Химические свойства азота:
- Не растворяется в воде
- Не горит и не поддерживает горение
- Образует связи с другими элементами и образует большое количество соединений
- Является необходимым элементом для формирования аминокислот и белка в живых организмах
Таким образом, азот - важный элемент, имеющий широкий спектр применения в различных отраслях науки и производства.
Молекулярная масса азота

Молекулярная масса азота равна примерно 14 г/моль, что означает, что одна моль азота содержит около 14 граммов. Это значение получается путем сложения атомных масс всех атомов, составляющих молекулу азота.
Масса одной молекулы азота равна примерно 2,3 x 10-23 грамма. Для определения массы 1022 молекул азота необходимо умножить массу одной молекулы на количество молекул.
Формула для рассчета:
Масса = количество молекул x масса одной молекулы
Таким образом, масса 1022 молекул азота равна примерно 2,3 x 10-1 г.
Молекулярная масса азота имеет большое значение в химических расчетах, так как она позволяет определить количество вещества и проводить различные преобразования между граммами и молями.
Как вычислить массу 10^22 молекул азота?

Масса молекулы азота (N2) составляет приблизительно 28 грамм/моль. Чтобы вычислить массу 1022 молекул азота, нужно умножить массу одной молекулы на количество молекул.
Вычислим:
| Масса одной молекулы азота (N2) | 28 г/моль |
| Количество молекул (1022) | 1022 молекул |
Умножение массы одной молекулы на количество молекул дает нам массу 1022 молекул азота:
Масса = масса молекулы x количество молекул
Масса = 28 г/моль x 1022 молекул
Масса = 2,8 x 1023 г
Таким образом, масса 1022 молекул азота равна 2,8 x 1023 грамма.
Значимость массы 10^22 молекул азота
Молекулы азота активно участвуют в химических реакциях, особенно в обмене веществ в организмах. Низкая масса 10^22 молекул азота может привести к нарушению таких важных процессов, как дыхание и пищеварение.
В атмосфере Земли азот составляет около 78% и выполняет функцию стабилизации климата. Благодаря этому элементу поддерживается баланс тепла и уровней влажности, что влияет на рост и развитие растений и животных.
Масса 10^22 молекул азота имеет значение не только для биологических систем, но и для промышленных процессов. Азот применяется в производстве различных химических соединений, удобрений, взрывчатых веществ и прочего.
Таким образом, масса 10^22 молекул азота важна для поддержания жизни на Земле, обеспечения нормального функционирования биологических систем и удовлетворения потребностей человека в различных отраслях деятельности.
Перспективы использования азота
В сельском хозяйстве азот применяется в качестве основного питательного элемента для растений. Он участвует в образовании аминокислот, белков и пигментов, что способствует росту растений и повышению их урожайности. Кроме того, азот используется в процессе азотной фиксации, который осуществляют некоторые виды бактерий, способные преобразовывать атмосферный азот в доступную для растений форму.
В промышленности азот широко применяется в процессах охлаждения и замораживания, так как он обладает способностью снижать температуру и поддерживать низкий уровень влажности. Это особенно важно для хранения и транспортировки пищевых продуктов, медицинских препаратов и других перишабельных материалов. Кроме того, азот используется в промышленности как инертный газ для предотвращения окисления и образования взрывоопасных смесей.
Азот также находит применение в производстве различных химических соединений, таких как аммиак, нитраты, нитриты и другие. Эти вещества широко используются в производстве удобрений, пищевых добавок, пиротехнических смесей, взрывчатых веществ и других продуктов. Аммиак, получаемый из азота, является основным сырьем для синтеза азотной кислоты, которая в свою очередь используется в медицине, производстве пластмасс, химических добавок и других отраслях промышленности.
Благодаря своей важной роли в сельском хозяйстве, промышленности и науке, азот становится все более востребованным ресурсом. Его уникальные свойства и широкий спектр применений делают его неотъемлемой частью современного общества.