Периодическая система химических элементов является одним из самых важных инструментов для науки о веществе. В ней каждый элемент имеет свой уникальный атомный номер, который определяет его положение в таблице Менделеева и отражает его структуру и химические свойства. Атомный номер является основной характеристикой элемента и является фундаментальным понятием в химии.
Атомный номер представляет собой число протонов в ядре атома элемента. Он указывает на количество электронов в нейтральном атоме, поскольку количество протонов и электронов в атоме всегда одинаково. Атомный номер также определяет порядковый номер элемента в периодической системе и позволяет упорядочивать элементы по возрастанию атомных номеров.
Атомный номер в периодической системе: понятие и значение
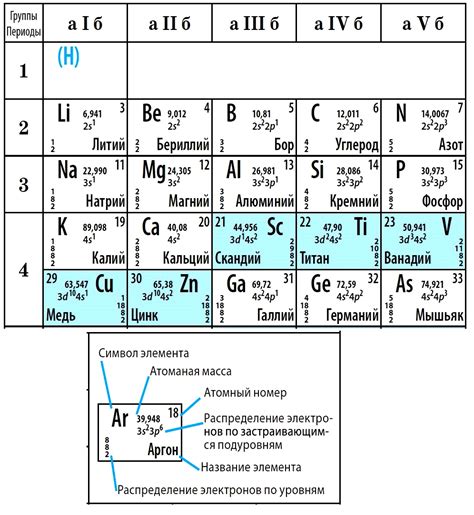
Атомный номер является уникальным для каждого элемента и служит основой для их систематизации. Он также определяет электронную конфигурацию элемента, его химические и физические свойства. С помощью атомного номера можно определить место элемента в периодической системе и его группу.
Знание атомного номера элемента позволяет предсказывать его реактивность, химические связи и реакции, а также свойства соединений, в которых он присутствует. Этот параметр также позволяет идентифицировать элементы по их символу и определять их массовое число.
Понимание значения атомного номера в периодической системе позволяет ученым и химикам проводить исследования, разрабатывать новые соединения и материалы, а также прогнозировать свойства и поведение элементов в различных реакциях и условиях.
Атомный номер: определение и особенности
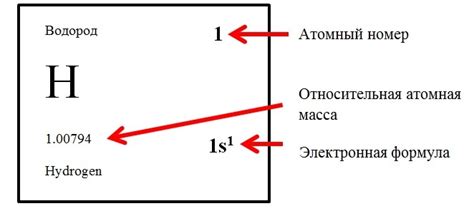
Атомный номер имеет важное значение в химии и физике, так как позволяет определить электронную конфигурацию атома и его химические свойства. Чем выше атомный номер, тем больше электронных оболочек и подуровней в атоме, что влияет на его реакционную способность и способность образовывать химические связи.
Атомный номер также определяет порядок размещения элементов в периодической системе. Элементы с атомными номерами, увеличивающимися слева направо и сверху вниз, располагаются в одинаковом порядке в каждом периоде и группе соответственно. Это обеспечивает удобство классификации элементов и позволяет предсказывать их свойства на основе их положения в периодической таблице.
Атомный номер является основным параметром, используемым для идентификации элементов и их обозначения. Каждый элемент имеет уникальный атомный номер, который обычно указывается над символом элемента в периодической таблице. Например, углерод имеет атомный номер 6, а кислород имеет атомный номер 8.
Важно отметить, что атомный номер может быть использован для определения других характеристик элемента, таких как его массовое число и атомная масса. Одно из главных свойств атома, его атомный номер необходим для понимания и изучения химических и физических свойств химических элементов.
Значение атомного номера для химических элементов
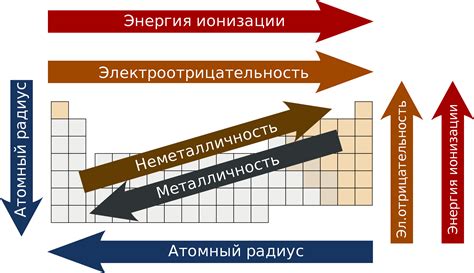
Атомный номер позволяет классифицировать элементы и определять их положение в периодической системе. Чем больше атомный номер, тем больше протонов в атоме и тем больше масса элемента. Таким образом, атомный номер прямо связан с химическими и физическими свойствами элементов.
В периодической системе Менделеева элементы расположены в порядке возрастания атомного номера. Такая организация позволяет легко найти информацию о каждом элементе – его название, символ, атомную массу и другие свойства.
Значение атомного номера для химических элементов уникально и не повторяется. Каждый элемент имеет свой уникальный атомный номер, который изначально устанавливается при открытии нового элемента или открытии новой химической реакции.
Атомный номер является важным показателем для изучения и понимания химических процессов и свойств различных веществ. Он помогает химикам и ученым классифицировать и систематизировать элементы, легко идентифицировать их и проводить дальнейшие исследования в области химии и материаловедения.
Атомный номер и строение атома

Атомы состоят из ядра и электронной оболочки. Ядро атома содержит протоны и нейтроны, а электронная оболочка – электроны. Протоны имеют положительный заряд, нейтроны не имеют заряда, а электроны имеют отрицательный заряд.
Атомный номер определяет количество протонов в ядре атома. Например, у атома водорода атомный номер равен 1, что означает наличие одного протона в ядре. Углерод имеет атомный номер 6, что означает наличие шести протонов в ядре.
Число протонов в атоме также определяет его атомную массу и место в периодической системе элементов. Атомы с одинаковым атомным номером, но разным числом нейтронов, называются изотопами. Изотопы могут иметь различные свойства и использоваться в разных областях науки и промышленности.
Влияние атомного номера на физические свойства элементов

Одним из важных свойств, зависящих от атомного номера, является атомный радиус. С увеличением атомного номера атомный радиус уменьшается. Это связано с тем, что с ростом атомного номера увеличивается количество протонов и электронов в атоме, что приводит к большему притяжению электронов к ядру и, как следствие, уменьшению размеров атома.
Другим физическим свойством, зависящим от атомного номера, является электроотрицательность. Электроотрицательность элемента характеризует его способность притягивать электроны, когда они образуют химическую связь. С увеличением атомного номера электроотрицательность элементов также растет, что делает эти элементы более активными и реакционноспособными.
Также атомный номер влияет на массовое число элемента, которое представляет собой сумму протонов и нейтронов в атомном ядре. Увеличение атомного номера приводит к увеличению массового числа элемента, что влияет на физические свойства, связанные с массой атома, такие как плотность или точка плавления.
В общем, атомный номер элемента в периодической системе является важным фактором, определяющим его физические свойства. Рассмотренные выше свойства, такие как атомный радиус, электроотрицательность и массовое число, являются только некоторыми из примеров влияния атомного номера на свойства элементов.
Атомный номер и химические свойства элементов
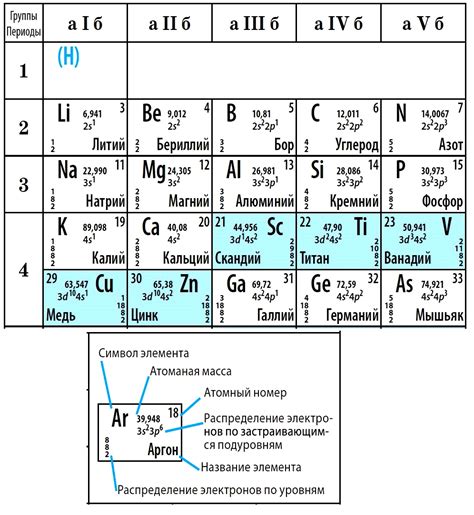
Атомный номер играет важную роль в определении химических свойств элементов. Химические свойства элементов определяются электронной структурой атомов и их взаимодействием с другими элементами.
Чем больше атомный номер элемента, тем больше его электронная оболочка и, следовательно, тем сложнее его химические свойства. Некоторые элементы малого атомного номера, такие как водород и гелий, имеют простую электронную структуру и обладают особыми химическими свойствами.
Атомный номер также помогает определить расположение элемента в периодической системе. По мере увеличения атомного номера элементы распределяются в порядке возрастания, образуя периоды и группы. Группы обладают схожими свойствами, так как элементы в одной группе имеют одинаковое количество валентных электронов.
Важно отметить, что атомный номер может изменяться по ходу периода. Например, углерод имеет атомный номер 6, а затем следует атомный номер 7 - азот.
| Элемент | Атомный номер | Химические свойства |
|---|---|---|
| Водород | 1 | Не имеет окрашенности, легко реагирует с кислородом и образует воду |
| Гелий | 2 | Инертен, не реагирует с другими элементами |
| Кислород | 8 | Реагирует с многими элементами, образует оксиды |
| Железо | 26 | Хороший проводник электричества и тепла, образует оксиды |
Таким образом, атомный номер играет ключевую роль в классификации и определении химических свойств элементов. Он помогает нам понять, как элементы взаимодействуют друг с другом и какие соединения они могут образовывать.
Систематика атомных номеров в периодической таблице
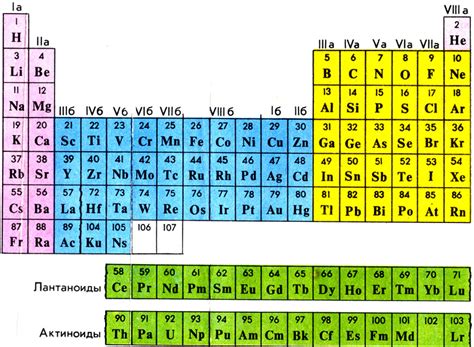
Атомный номер представляет собой порядковый номер элемента в периодической таблице. Он определяет количество протонов в ядре атома данного элемента и указывает на его положение в таблице. Чем выше атомный номер, тем больше протонов имеет атом и тем больше его атомная масса.
Систематика атомных номеров в периодической таблице основывается на принципе упорядочивания элементов по возрастанию атомного номера. Каждый новый элемент имеет на единицу больший атомный номер по сравнению с предыдущим элементом.
Периодическая таблица состоит из семи горизонтальных строк, называемых периодами, и 18 вертикальных столбцов, называемых группами. Группы обозначаются номерами от 1 до 18, а периоды обозначаются номерами от 1 до 7. Атомные номера элементов в периодической таблице помещаются в ячейки, которые соответствуют их положению в таблице.
Систематика атомных номеров в периодической таблице важна для понимания связей между различными элементами и их химическими свойствами. Она позволяет классифицировать элементы по группам и периодам, что помогает в изучении и прогнозировании их реакционной способности и влияния на окружающую среду.
Значение атомного номера для определения химической реактивности

Значение атомного номера влияет на химическую реактивность элемента. Большинство элементов с малым атомным номером имеют низкую реактивность и редко участвуют в химических реакциях. Например, элементы с атомными номерами от 1 до 10 (водород, гелий, литий и т.д.) химически пассивны и не образуют стабильные соединения с другими элементами. Элементы с атомными номерами от 11 до 18 (натрий, магний, кислород и т.д.) имеют более высокую реактивность и образуют широкий спектр соединений с другими элементами.
Наиболее высокую химическую реактивность обычно проявляют элементы с неполной внешней электронной оболочкой (например, элементы из 1 и 2 групп периодической системы). Они стремятся завершить свою оболочку, потеряв или приобретая один или несколько электронов. Это приводит к образованию ионов с положительными или отрицательными зарядами и возникновению химических реакций.
Таким образом, значение атомного номера в периодической системе элементов является важным фактором для определения химической реактивности элементов. Чем выше атомный номер, тем выше реактивность элемента и его способность образовывать стабильные соединения с другими элементами.